
Ферменты
Ферменты - это катализаторы биохимических реакций. Питание и дыхание микробной клетки связано с работой ферментов. Они обусловливают способность живых организмов осуществлять превращение веществ, необходимых для их жизнедеятельности.
Ферменты синтезируются только живыми клетками, мертвые клетки их не образуют. Ферменты высокоспецифичны. Каждый фермент ускоряет только одну или группу сходных между собой химических реакций.
Очень небольшое количество ферментов вызывает превращения огромного количества вещества, но сами ферменты при этом не расходуются. Ферменты вступают в соединение с субстратом и участвуют в самом превращении вещества, но в конце реакции освобождаются в неизменном виде.
Ферменты разделяются по своему строению на две группы: однокомпонентные и двухкомпонентные. Однокомпонентные ферменты - это кристаллические белки протеины (уреаза, пепсин и др.), активность их в основном обусловливается определенным расположением аминокислот в молекуле белка. Двухкомпонентные ферменты имеют две составные группы: активная простетическая (кофермент) и коллоидный белковый носитель.
Первая группа непосредственно участвует в ферментной реакции. Коллоидный же белковый носитель увеличивает активность фермента, определяет специфичность его действия. Простетическая группа обычно содержит те или иные витамины или металлы (железо, медь, магний и др.).
Ферменты снижают энергию активизации, осуществляющую химическую реакцию, направляя ее обходным путем через промежуточные реакции, требующие значительно меньшей активизации. В условиях организма почти всегда действует целая группа ферментов, разбивающих процесс превращения вещества на большое число ступеней, так, например, превращение сахара в спирт проводится десятью последовательно действующими ферментами. Каждый фермент вызывает определенное изменение одного вещества. Продукт одной ферментативной реакции служит субстратом для последующей ферментативной реакции. Образованное новое вещество подвергается последовательно действию следующего фермента. Последовательность действия ферментов обеспечивается тем, что ферменты строго локализованы на определенных структурах клетки. Благодаря этому наблюдается необычайная согласованность действия отдельных ферментов, приводящих к поразительной слаженности всех обменных реакций.
Микробы имеют те же ферменты, что и растения. Но есть ряд ферментов, встречающихся только у микробов, например целлюлаза, гидролизирующая клетчатку корма в желудке жвачных, фиксация атмосферного азота происходит в результате действия специфических ферментных систем, которых нет у животных и высших растений.
Одни ферменты проявляют свое действие только внутри микробной клетки, например дегидразы, оксидазы (эндоферменты), другие выделяются клеткой во внешнюю среду (эктоферменты), где разлагают сложные органические соединения (крахмал, клетчатку) до более простых, проходимых через оболочку клетки, к последним относятся гидролазы. Название гидролитических ферментов составляется из названия расщепляемого ими вещества с приставкой на конце -аза (лактаза, мальтаза и др.). Ферменты, вызывающие глубокий распад органического вещества, получают названия по характеру их действия - оксидаза, дегидраза и пр.
К гидролазам относятся: 1) карбоназы, разлагающие поли- и дисахариды; 2) липазы, расщепляющие жиры, и 3) протеазы, расщепляющие белки до пептонов, полипептиды - до дипептидов и аминокислот, мочевину - до аммиака и углекислоты.
Окислительно-восстановительные ферменты осуществляют перенос водорода и кислорода в процессе дыхания. Вещество, отдающее водород, называется донатором водорода, а вещество, принимающее водород, - акцептором. Отдающее водород (электрон) вещество окисляется, получающее водород (электрон) - восстанавливается. Из окислительно-восстановительных ферментов дегидразы активизируют водород и переносят его от одной молекулы органического вещества к другой. Оксидазы активизируют и переносят молекулярный кислород. Цитохромная система с цитохромоксидазой является промежуточным звеном между дегидрогеназами и кислородом воздуха. Цитохромы имеются только у аэробов и отсутствуют у анаэробов. Цитохромы относятся к порфириновым коферментам, каковыми являются хлорофилл, гемоглобин. Они составляют группу желтых пигментов, содержащих железо и очень напоминающих тем - вещество, придающее крови красный цвет. Атом железа попеременно окисляется и восстанавливается, превращаясь из Fe++ в Fe+++ и обратно, отдавая или принимая один электрон.
Из химических соединений, входящих в коферменты, наиболее важное значение имеют гемин, тимин, флавин, аденин, пиридин. Но эти соединения в коферменте должны находиться в нуклеотидной форме, т. е. соединены с азотистым основанием рибозой и фосфорной кислотой. В этой форме происходит взаимодействие между коферментом и специфическим белком. Так, в состав анаэробных дегидраз входит кофермент ди- или трифосфопиридиннуклеотид (НАД или НАДФ), действующее начало в нем витамин никотинамид (ниацин). В аэробной дегидразе коферментом является флавинадениннуклеотид (ФАД), он содержит витамин флавин (В2). Имеется много других подобных коферментов.
Коферменты, участвующие в аккумуляции и переносе энергии, представляют адениловую систему, строение ее показано на схеме ниже. В составе аденозинтрифосфорной кислоты имеются две макроэргические фосфатные связи (обозначенные знаком ~), каждая по 10-16 тысяч калорий, тогда как в обычных эфирных связях содержится всего по 2-3 тысячи калорий.
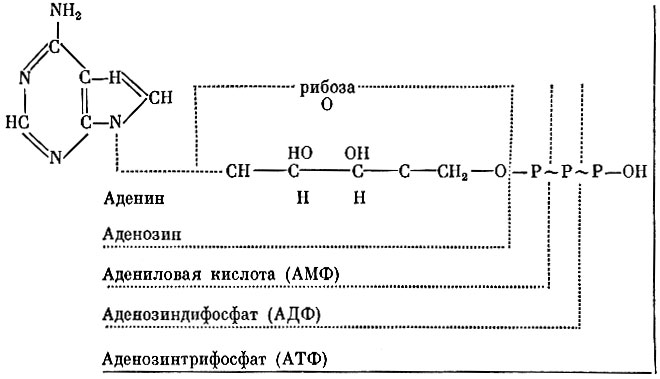
Схема
Макроэргическую связь в 8 тысяч калорий содержит кофермент А, но не с фосфором, а с серой. Кофермент содержит витамин пантотеновую кислоту. Он служит переносчиком остатков уксусной и других кислот, конденсирует уксусную кислоту со щавелевоуксусной кислотой, в результате чего образуется лимонная кислота.
Ферменты синтеза называются синтетазами и литазами. Академик А. И. Опарин показал, что гидролитическое действие ферментов осуществляется в гомогенном растворе.
Ферментативная деятельность микробов имеет огромное практическое значение в промышленной технологии виноделия, пивоварения, хлебопечения, в получении спиртов, щавелевой, молочной кислот, глицерина и пр. Многие ферменты применяются как лечебные средства.

Таблица 3. Ферменты микроорганизмов, имеющие важное значение в промышленности (по Фробишеру)
Определение ферментативных свойств используется в систематике микробов при определении видов микроорганизмов.
Подробные сведения о ферментах можно найти в руководствах по биологической химии.
|
ПОИСК:
|
© BIOLOGYLIB.RU, 2001-2020
При копировании ссылка обязательна:
http://biologylib.ru/ 'Библиотека по биологии'
При копировании ссылка обязательна:
http://biologylib.ru/ 'Библиотека по биологии'