
7. Неорганический синтез "органических" соединений в условиях примитивной атмосферы
Но нам не так уж важен точный состав примитивной атмосферы и гидросферы. Важно, что на Земле не было свободного кислорода и были сравнительно простые абиогенные соединения углерода с другими элементами, такими, как О, Н, N, S, Р и другие (фиг. 13). Сейчас такие соединения можно найти только в живых организмах или в продуктах их жизнедеятельности. Наряду с ними встречались и другие абиогенные соединения, такие, как СО, СО2, Н2О, SiО2, силикаты, сульфаты и т. д., - они и сейчас образуются абиогенным путем.
![Фиг. 13. Строение малых молекул, которые неизбежно должны присутствовать в любой планетной примитивной атмосфере и гидросфере [6]. Объединяясь, они образуют более крупные 'органические' молекулы, а те в свою очередь могут служить строительными блоками для еще более крупных молекул жизни (более подробно об этом - в гл. VI)](pic/000020.jpg)
Фиг. 13. Строение малых молекул, которые неизбежно должны присутствовать в любой планетной примитивной атмосфере и гидросфере [6]. Объединяясь, они образуют более крупные 'органические' молекулы, а те в свою очередь могут служить строительными блоками для еще более крупных молекул жизни (более подробно об этом - в гл. VI)
Соединения углерода дважды обязаны своим возникновением отсутствию свободного кислорода. Во-первых, только в условиях бескислородной атмосферы они и могли образоваться абиогенным способом, тогда как в современных условиях лишь процессы жизни дают необходимую для таких синтезов энергию. Во-вторых, только в бескислородных условиях они могли оставаться стабильными или хотя бы разрушаться медленнее, чем шел их синтез. Ведь в бескислородной атмосфере, как мы помним, не протекали процессы окисления и органического разложения.
Почему же простые "органические" соединения могли создаваться неорганическим путем? Дело в том, что тогда не было кислородно-озонового экрана, поглощающего самые коротковолновые ультрафиолетовые лучи Солнца. Эти лучи свободно проходили через бескислородную атмосферу и падали на поверхность Земли. Такое коротковолновое излучение несет очень большую энергию. Оно вызывало неорганические фотохимические реакции, невозможные теперь, под защитой озонового экрана. Коротковолновая часть ультрафиолетового излучения Солнца настолько богата энергией, что она вынуждала элементы атмосферы и гидросферы образовывать химические связи, т. е. образовывать после поглощения световых квантов молекулярные соединения (фиг. 14). Конечно, это неорганический процесс, но, как мы увидим в гл. VI, он может давать начало типичным "органическим" молекулам. Поскольку процесс этот основан на поглощении квантов света, идущих от Солнца, его можно назвать фотосинтезом. Но это неорганический фотосинтез. Не путайте его с органическим фотосинтезом, который протекает сейчас в растениях при участии хлорофилла. В органическом фотосинтезе используется главным образом энергия квантов красной части спектра. Она не так велика, и все же благодаря тому, что процесс разбит на множество последовательных стадий, растениям удается синтезировать те же органические соединения, которые создавались за счет энергии ультрафиолетового излучения без участия организмов. Каждая стадия реакции требует гораздо меньше энергии, чем весь процесс, поэтому растения могут использовать красную часть спектра, несущую гораздо меньше энергии, чем ультрафиолет.
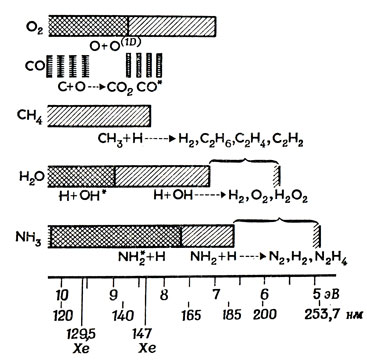
Фиг. 14. Фотохимические реакции, идущие в различных газах при облучении их светом с разной длиной волны. Кислород поглощает ультрафиолетовые лучи с длиной волны 185 нм и менее. Энергия световых квантов этого участка спектра возрастает с 7 эВ (для 180 нм) до 10 эВ (для 120 нм). Свет этой области спектра активирует и другие газы - СО, СО2, СН4, Н2О и NH3, что показано столбиками с различной штриховкой. Звездочки, поставленные у некоторых радикалов, отмечают длину волны, при которой эти радикалы начинают светиться. Это их свойство не имеет значения для синтеза молекулярных соединений, но важно для определения данных радикалов в эксперименте. Пунктирными стрелками указаны участки спектра, в которых из атомов и радикалов образуются сложные молекулы. Две линии ксенона - 129,5 и 147 нм - указывают области строго монохроматического излучения ксеноновой лампы, которую Грот еще в 1938 году использовал в подобных экспериментах. Значит, наша современная атмосфера непрозрачна для тех длин волн, которые активируют простые устойчивые газообразные соединения, такие, как СО, СН4, Н2О и NH3. Следовательно, в современной атмосфере из этих газов не могут путем неорганического фотосинтеза образоваться более сложные соединения, так как наиболее коротковолновое солнечное излучение не достигает поверхности Земли. Но водород совершенно прозрачен для такого излучения, и поэтому в атмосфере, состоящей главным образом из водорода, оно беспрепятственно проникало бы до поверхности Земли
Как уже говорилось, мы не знаем точного состава примитивной атмосферы. Точно так же мы не имеем ясного представления о составе, количестве и концентрации простых соединений углерода с другими элементами, создававшихся за счет неорганических процессов в бескислородной атмосфере и на поверхности Земли. Многие ученые, особенно химики-органики [6], считают, что среди них были такие реакционноспособные вещества, как цианистый водород (или синильная кислота), а также дицианамид и их производные. Гидросфера представляла собой смесь воды с этими веществами. Часто эту смесь изображают как нечто вроде "жидкого бульона", что избавляет от необходимости подробнее описать ее состав.
Нелегко подыскать подходящее название для жидкости, из которой состояла ранняя гидросфера. В ней содержались "органические" молекулы, созданные чисто неорганическими, или, если вам этот термин нравится больше, абиогенными, процессами. Эту жидкость часто сравнивают с бульоном потому, что малые "органические" молекулы, встречавшиеся в ней, служили пищей для развивавшейся жизни. Впрочем, некоторые авторы считают термин "бульон" чересчур обиходным и предпочитают говорить о "предбиологическом", "добиологическом" или "питательном" бульоне. Опарин [20] использует термин "первичный бульон". Я думаю, что представление о "жидком бульоне" уже так широко распространено (в том числе и среди неспециалистов), что его можно использовать и в дальнейшем. Кавычки напоминают, что этот бульон был мало похож на обычный.
Его особенности мы рассмотрим позже. Философ Д. Гаукинс [10] назвал этот бульон "чем-то вроде водного Эдема" - ведь тогда в любой капле океана жизнь могла найти все необходимое на этой ранней стадии чисто химической эволюции.
Как мы увидим в гл. XVI, весьма вероятно, что химические реакции, приводящие к образованию "бульона", шли долгое время и после того, как на Земле возникла жизнь. На заре своего развития жизнь могла сосуществовать с преджизнью в течение примерно 2 млрд. лет, наслаждаясь изобилием этого первобытного рая. Тогда в пищу живому шли "органические" молекулы, синтезированные неорганическим путем.
|
ПОИСК:
|
© BIOLOGYLIB.RU, 2001-2020
При копировании ссылка обязательна:
http://biologylib.ru/ 'Библиотека по биологии'
При копировании ссылка обязательна:
http://biologylib.ru/ 'Библиотека по биологии'