
Витамин B1 (тиамин)
В конце прошлого века тысячи моряков на японских судах страдали, а многие из них умирали мучительной смертью от таинственной болезни, называвшейся "бери-бери". Одной из загадок бери-бери было то, что моряки на судах других стран этой болезнью не болели.
В 1882 г. японский морской врач Канегиро Такаки в своей работе, вполне заслуживающей названия "медицинского детектива", показал, что решение проблемы борьбы с этой болезнью заключается в правильном питании. Он обнаружил, что замена очищенного риса, составлявшего в основном рацион питания японских моряков, неочищенным не только помогает излечиться от болезни, но и предотвращает ее появление. Такаки предположил, что в рисовой шелухе содержатся какие-то важные белки, которых недоставало в пище болевших матросов.
Последующая работа показала, что такое предположение правильно лишь отчасти. В рисовой шелухе действительно находится существенно важный для правильного питания фактор, однако вещество это не является белком. Это небольшая органическая молекула, называемая тиамином, который служит коферментом, т. е. действует вместе с ферментом (являющимся белком), катализируя специфические обменные химические реакции.
Одной из важных обменных реакций, требующих участия тиамина, является реакция декарбоксилирования пировиноградной кислоты
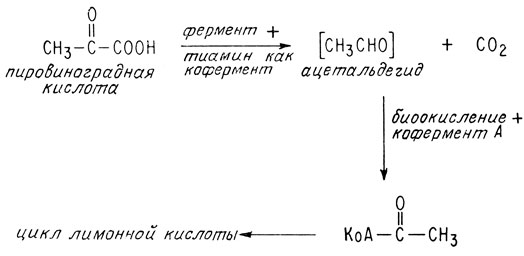
В гл. 2 было показано, что эта реакция "питает" цикл образования лимонной кислоты - очень важную последовательность реакций, которая служит источником энергии для живых систем, ведущих аэробный образ жизни. Не удивительно, что недостаток тиамина приводит к сильнейшему клеточному истощению*.
* (Тиамин - единственный из известных коферментов, для которого диагноз надвигающегося недостатка витамина можно поставить химическим путем, до того как разовьется болезнь бери-бери.)
Растения могут синтезировать тиамин, а животные и человек такой способностью не обладают; некоторые бактерии и грибы также не способны синтезировать тиамин. Таким образом, и животные, и человек должны получать тиамин с пищей, и, поскольку соединение это не относится ни к белкам, ни к углеводам, ни к жирам, его назвали витамином и произвольно обозначили как витамин B1. Большое количество этого витамина содержат яйца, мясо, горох и бобы. Суточная потребность человека составляет 1-3 мг витамина В1.
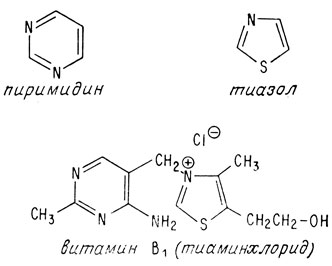
Впервые витамин B1 был выделен в 1926 г. из рисовой шелухи. Спустя десять лет была установлена его структура и осуществлен синтез. Молекула этого витамина состоит из двух циклических компонентов, соединенных мостиком из одного атома углерода. В этом смысле она напоминает молекулу хинина. Однако циклические компоненты тиамина отличаются от компонентов хинина. Тиамин содержит пиримидиновое кольцо (которое уже встречалось, когда речь шла о нуклеиновых кислотах) и кольцо тиазола. Тиазольное кольцо содержит атом серы и атом азота.
Установление структуры витамина B1 не представляло особых трудностей еще и потому, что его молекулу можно расщепить на две части в очень мягких условиях. Сульфит-ион в почти нейтральном водном растворе атакует мостиковый атом углерода, в результате чего освобождается тиазольное кольцо
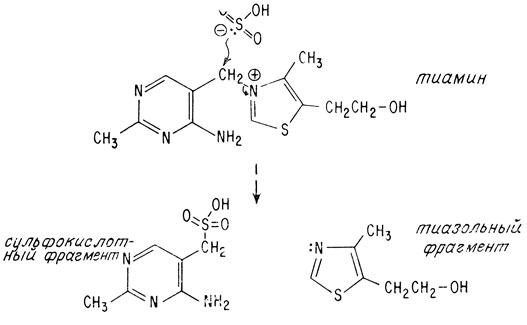
Мостиковый углеродный атом тиамина подвержен нуклеофильной атаке вследствие мощного электроноакцепторного воздействия положительно заряженного атома азота. Сульфогруппу можно удалить действием раствора металлического натрия в безводном жидком аммиаке
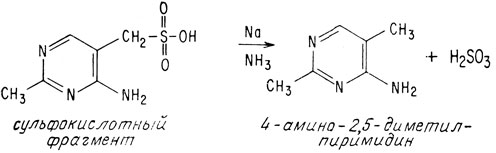
Ультрафиолетовые спектры как сульфокислотного производного, так и продукта его восстановления показали, что эти соединения могли бы быть пиримидинами; такая их структура впоследствии была подтверждена синтезом.
На основании ультрафиолетовых спектров также предположили, что другая часть молекулы, получаемая в результате разложения молекулы под действием сульфита, может содержать тиазольное кольцо. При окислении этого фрагмента азотной кислотой получилось известное производное тиазола 4-метилтиазол-5-карбо-новая кислота
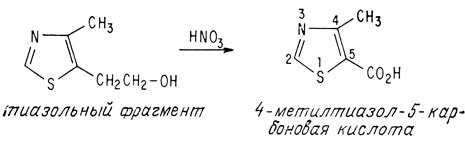
Тиазольный фрагмент до окисления азотной кислотой не содержит карбоксильной группы, а потому атом углерода, входящий в карбоксильную группу, должен изменяться в процессе этой реакции. Согласно данным элементного анализа, до окисления этот фрагмент содержал шесть атомов углерода и лишь один атом кислорода. Известно, что этот атом кислорода входит в гидроксильную группу, поскольку он может образовать сложный эфир. Все эти данные указывают на две возможные структуры тиазольного фрагмента - одну с первичной спиртовой группой, другую со вторичной спиртовой группой.
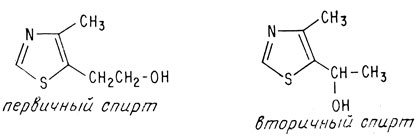
Первичные и вторичные спирты можно легко различить при помощи простых химических реакций. Эти реакции показали, что в тиазольном фрагменте содержится первичная спиртовая группа. Структура, включающая вторичную спиртовую группу, имеет также асимметричный углеродный атом, а потому ее можно было бы разделить на оптически активные фракции. Однако тиазольный фрагмент на оптически активные антиподы не разделяется. Синтез структуры, содержащей первичную спиртовую группу, подтвердил ее идентичность с тиазольным фрагментом.
Этим завершается установление структуры обоих фрагментов молекулы тиамина, однако вопрос о том, как же эти фрагменты связаны друг с другом, остается без ответа. На характер соединения этих фрагментов друг с другом указывают следующие данные. Во-первых, молекула тиамина не содержит сульфогруппы, поэтому атом углерода, сульфируемый сульфит-ионом, должен участвовать в соединении фрагментов. Во-вторых, издавна известно, что тиамин является четвертичным аммониевым соединением, т. е. существует в виде соли. Единственным атомом азота, который может отвечать этим требованиям и способен связать оба фрагмента, является атом азота тиазола. Следовательно, мостиковый атом углерода должен быть присоединен к атому азота тиазола, как показано ниже:
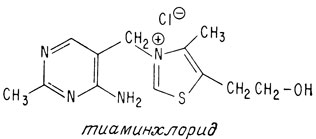
Теперь, когда структура тиамина установлена, интересно узнать, как он действует в организме в роли витамина. Мы уже говорили о том, что он представляет собой кофермент, участвующий в реакции декарбоксилирования пировиноградной кислоты, питающей важнейший цикл лимонной кислоты. В качестве кофермента тиамин присутствует во всех живых клетках в виде эфира пирофосфорной кислоты
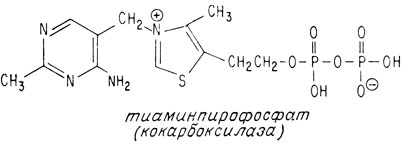
Этот кофермент называется кокарбоксилазой, поскольку он действует совместно с ферментом карбоксилазой, катализирующей декарбоксилирование пировиноградной кислоты. Полностью ферментативная система состоит из белка с молекулярным весом около 150000, одной молекулы кофермента и пяти атомов магния.
Активным центром кофермента считают атом углерода, расположенный между атомом серы и четвертичным атомом азота
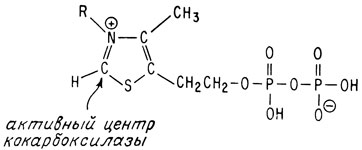
Этот атом углерода сначала теряет протон и становится отрицательно заряженным нуклеофилом
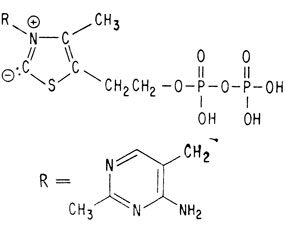
В качестве нуклеофила он может атаковать входящий в кетогруппу углеродный атом аниона пировиноградной кислоты (R-радикал, изображенный выше)
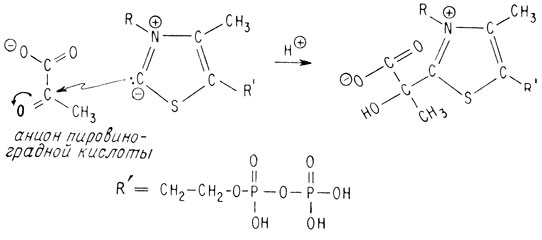
Мощное электроноакцепторное воздействие положительно заряженного четвертичного атома азота облегчает в этом случае декарбоксилирование аниона пировиноградной кислоты
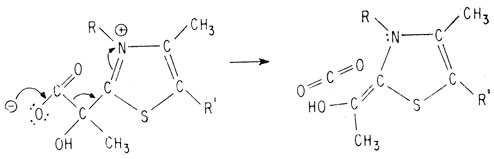
Восстановление системы сопряженных двойных связей тиазольного кольца приводит к образованию стабильного карбаниона
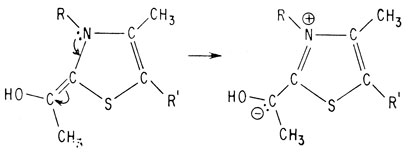
В этой молекуле возможен сдвиг протона и высвобождение продукта декарбоксилирования, в результате чего вновь получается исходный тиазол, являющийся нуклеофилом
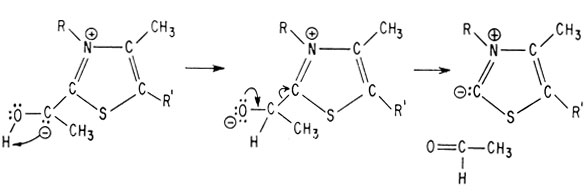
В пользу такого механизма действия витамина B1 свидетельствуют два факта. Во-первых, было синтезировано одно из приведенных выше промежуточных соединений - оксиэтилтиамин, которое по биологической активности почти не отличается от самого витамина B1
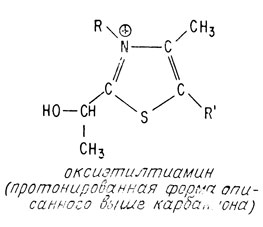
Во-вторых, это промежуточное соединение было выделено из микроорганизмов.
Как показано в суммарной реакции цикла лимонной кислоты в гл. 2, образующийся ацетальдегид затем окисляется и включается в цикл.
|
ПОИСК:
|
© BIOLOGYLIB.RU, 2001-2020
При копировании ссылка обязательна:
http://biologylib.ru/ 'Библиотека по биологии'
При копировании ссылка обязательна:
http://biologylib.ru/ 'Библиотека по биологии'