
Механизм инактивации электронотранспортной цепи изолированных хлоропластов
В работах [501, 502, 511] в рамках развитой выше кинетической модели проанализирован механизм инактивации электротранспортной цепи изолированных хлоропластов. Вопросы, требующие решения, можно сформулировать следующим образом. Что собой представляют процессы, характеризуемые константами k1, λ1, λ2? Какова их физическая природа? Какое звено в электронотранспортной цепи наиболее слабо, подвержено наиболее быстрой инактивации?
Детальное экспериментальное исследование процесса инактивации электронотранспортной цепи хлоропластов позволяет с определенной степенью достоверности ответить на эти вопросы. Были исследованы зависимости кинетики инактивации хлоропластов от pH, температуры, ионной силы раствора, природы и состава буферных солей, состава газовой фазы.
В процессе "старения" хлоропластов наблюдается увеличение их активности. Характеристическое время этого процесса включает в себя константу k1. Можно было бы думать, что этот эффект связан с увеличением в процессе денатурации мембраны хлоропластов доступности доноров электронотранспортной цепи для феррицианид-иона. В этом случае в начальный момент времени система должна работать в диффузионном режиме по феррицианид-иону и скорость реакции должна зависеть от его концентрации [466]. Экспериментальное исследование стационарной скорости электронного транспорта показало, что при используемых концентрациях феррицианида калия скорость процесса не зависит от его концентрации [511] (рис. 51). Этот факт показывает, что активация процесса не связана с простым физическим механизмом, облегчающим доступ для акцептора электронотранспортной цепи в процессе "старения" мембраны хлоропластов.
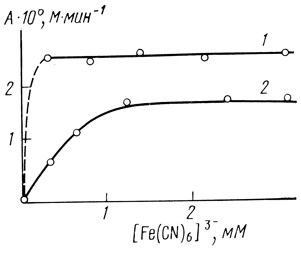
Рис. 51. Зависимость скорости фотоокисления воды электронотранспортной цепью изолированных хлоропластов от концентрации акцептора электронов: 1 - нативные хлоропласты; 2 - хлоропласты, иммобилизованные в 3%-ном агар-агаровом геле. Условия: 20% глицерина; 50 мМ хлористого натрия; хлоропласты в концентрации, соответствующей 2 мг/л хлорофилла; pH 7,6; 22°С
Существенному пониманию механизма процесса, характеризуемого константой k1, способствовало проведение кинетической корреляции между процессом активации хлоропластов в процессе "старения" и потерей способности мембраны хлоропластов к энергизации. Оказалось, что константа скорости инактивации способности мембраны к энергизации в пределах ошибки эксперимента совпадает с константой активации хлоропластов ("быстрая" экспонента на кинетической кривой инактивации хлоропластов (см. рис. 50)). Таким образом, процесс активации хлоропластов связан с потерей мембраной хлоропластов способности удерживать трансмембранный потенциал. В процессе "старения" хлоропластов происходит разобщение электронного транспорта и фосфорилирования, при этом возрастают скорости электронотранспортных процессов. Экспериментально показано, что добавление "классических" разобщителей приводит к активации электронного транспорта, по масштабам соизмеримой с "активацией" хлоропластов в процессе старения [502].
Принципиальным является выяснение природы процесса, характеризуемого константой λ2 (схема 3.103). С целью выяснения участка электронотранспортной цепи, ответственного за этот инактивационный процесс, было проведено сравнение процесса "старения" различных участков электронотранспортной цепи. При использовании экзогенных акцепторов электронов различных классов можно акцептировать электроны на уровне фотосистемы I или фотосистемы II. Кроме того, электроны можно донировать в электронотранспортную цепь на различных участках цепи. Для этой цели использованы феррицианид калия (акцептор I класса), 2,6-дихлорфенолиндофенол (акцептор II класса), n-бензохинон (акцептор III класса), а также смесь 2,5-дибром-3-метил-6-изопропилбензохинона с ферридианидом калия. Указанные соединения акцептируют электроны из различных участков электронотранспортной цепи. Сравнение кинетики инактивации по константе λ2 при использовании акцепторов фотосистемы I и акцепторов фотосистемы II показывает, что процесс инактивации характеризуется одним и тем же параметром λ2 (табл. 30). Это говорит о том, что центр инактивации расположен на общем участке электронотранспортной цепи, т. е. в восстановительной цепи фотосистемы II (система разложения воды). Этот вывод подтверждается тем фактом, что при использовании в качестве донора 1,5-дифенилкарбозида, донирующего электроны на переносчики системы разложения воды [512], экспериментально определяемый параметр λ2 существенно ниже (τ2 в отсутствие и в присутствии 1,5-дифенилкарбазида равны соответственно 1,5 ± 0,1 ч и 4,2 ± 0,2 ч, 32°С).

Таблица 30. Зависимость параметра λ2 от характера акцептора, снимающего электроны на различных участках электронотранспортной цепи
Таким образом, наиболее лабильный участок электронотранспортной цепи расположен в системе разложения воды до места донирования электронов дифенилкарбазидом. Этот вывод согласуется с рядом сведений биохимического характера [513].
Проведенное кинетическое исследование позволило выявить наиболее слабое, лабильное звено электронотранспортной цепи фотосинтеза. В дальнейшем работа была направлена на стабилизацию цепи электронного транспорта в хлоропластах.
|
ПОИСК:
|
© BIOLOGYLIB.RU, 2001-2020
При копировании ссылка обязательна:
http://biologylib.ru/ 'Библиотека по биологии'
При копировании ссылка обязательна:
http://biologylib.ru/ 'Библиотека по биологии'