
5.5.3. Структура белков
Каждому белку свойственна своя особая геометрическая форма, или конформация. При описании трехмерной структуры белков рассматривают обычно четыре разных уровня организации, которые мы здесь и опишем.
Первичная структура
Под первичной структурой белка понимают число и последовательность аминокислот, соединенных друг с другом пептидными связями в полипептидной цепи (рис. 5.31). Первые исследования по выяснению аминокислотной последовательности белков были выполнены в Кембриджском университете Ф. Сэнгером, дважды удостоенным за свои работы Нобелевской премии. Сэнгер работал с гормоном инсулином (рис. 5.32), и это был первый белок, для которого удалось выяснить аминокислотную последовательность. Работа заняла ровно 10 лет (1944-1954 гг.). В молекулу инсулина входит 51 аминокислота, а молекулярная масса этого белка равна 5733. Молекула состоит из двух полипептидных цепей, удерживаемых вместе дисульфидными мостиками.
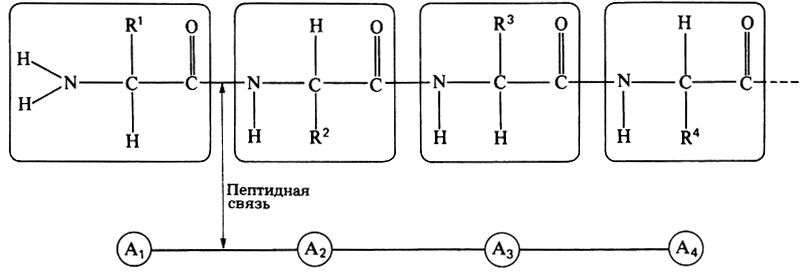
Рис. 5.31. Часть полипептидной цепи, представленная с целью показать первичную структуру. А1 А2, А3 и А4 - различные аминокислоты
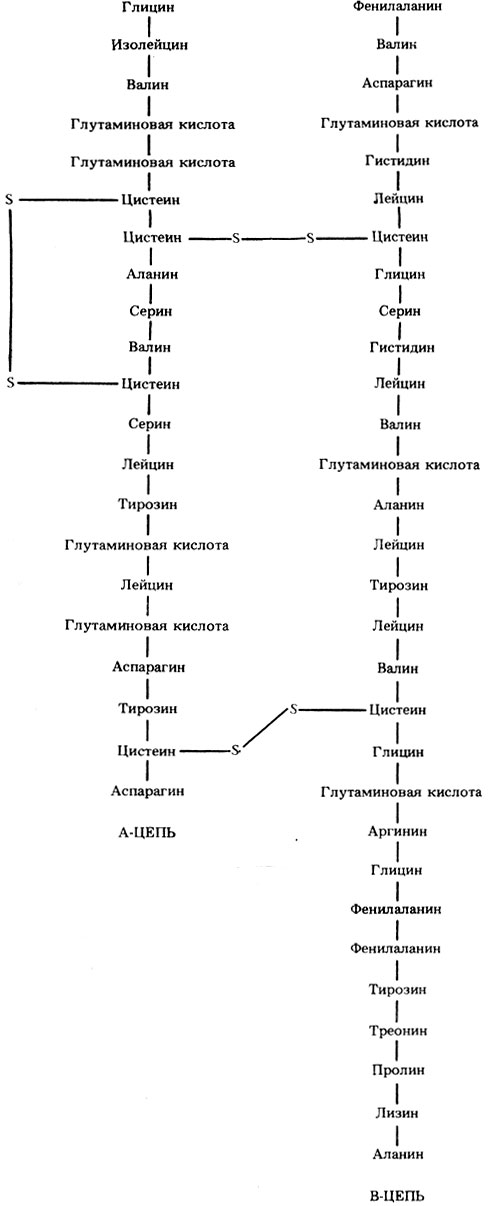
Рис. 5.32. Первичная структура (аминокислотная последовательность) инсулина. Молекула состоит из двух полипептидных цепей, удерживаемых вместе двумя дисульфидными мостиками
В настоящее время большая часть работ по определению аминокислотных последовательностей автоматизирована, и теперь первичная структура известна уже для нескольких сотен белков. На рис. 5.33 изображена первичная структура фермента лизоцима.
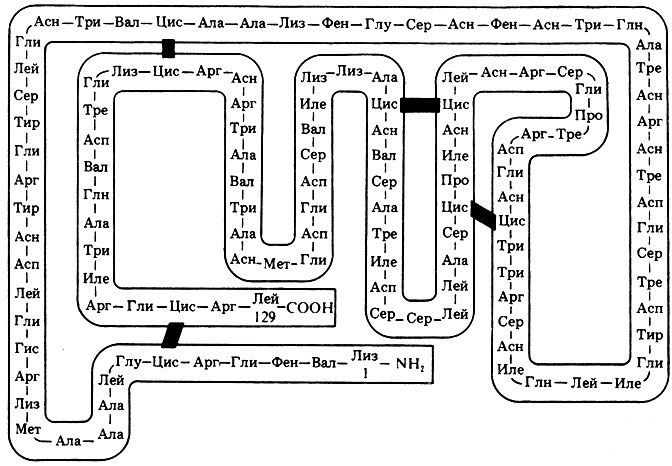
Рис. 5.33. Первичная структура лизоцима. Лизоцим - это фермент, обнаруженный во многих тканях и секретах человеческого тела, в растениях и яичном белке. Этот фермент катализирует разрушение клеточных стенок бактерий. Молекула лизоцима состоит из одной пол и пептидной цепи, в которую входит 129 аминокислотных остатков. В молекуле имеется четыре внутрицепочечных дисульфидных мостика
В организме человека свыше 10000 различных белков, и все они построены из одних и тех же 20 стандартных аминокислот. Аминокислотная последовательность белка определяет его биологическую функцию. В свою очередь эта аминокислотная последовательность однозначно определяется нуклеотидной последовательностью ДНК (разд. 22.6). Замена одной - единственной аминокислоты в молекулах данного белка может резко изменить его функцию, как это наблюдается, например, при так называемой серповидноклеточной анемии (разд. 23.9). Интересные данные могут быть получены в результате анализа аминокислотных последовательностей гомологичных белков, принадлежащих разным биологическим видам; такие данные позволяют судить о возможном таксономическом родстве между этими видами. Вопрос этот будет обсуждаться в гл. 24.
5.17. а) Напишите аминокислотные последовательности всех трипептидов, которые можно построить из двух разных аминокислот А и В.
б) Исходя из того, что у вас при этом получилось, составьте формулу для определения числа различных трипептидов, которые могут быть построены из двух разных аминокислот.
в) Сколько полипептидов длиной в 100 аминокислотных остатков можно построить из двух разных аминокислот?
г) Сколько полипептидов длиной в 100 аминокислотных остатков (а это сравнительно небольшой белок) можно построить из всех 20 стандартных аминокислот?
д) Сколько пептидов или полипептидов (заданной длины) можно построить из всех 20 стандартных аминокислот?
Вторичная структура
Для всякого белка характерна помимо первичной еще и определенная вторичная структура. Обычно белковая молекула напоминает растянутую пружину. Это так называемая α-спираль, стабилизируемая множеством водородных связей, возникающих между находящимися поблизости друг от друга СО- и NH-группами. Атом водорода NH-группы одной аминокислоты образует такую связь с атомом кислорода СО-группы другой аминокислоты, отстоящей от первой на четыре аминокислотных остатка (считая вдоль цепи назад) (рис. 5.34). Рентгеноструктурный анализ показывает, что на один виток спирали приходится 3,6 аминокислотного остатка.
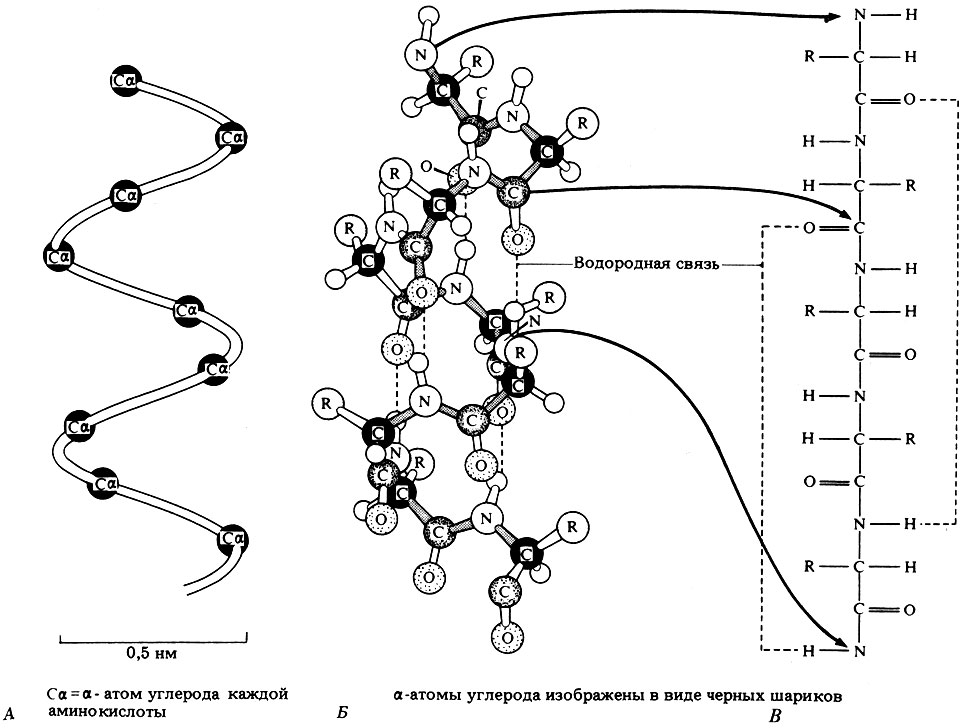
Рис. 5.34. Структура α-спирали. А. Показаны α-атомы углерода. Соединяющая их линия описывает α-спираль. Б. Модель α-спирали из стержней и шариков. В. Часть α-спирали в растянутом виде. Спираль стабилизируется водородными связями
Полностью α-спиральную конформацию и, следовательно, фибриллярную структуру имеет белок кератин. Это структурный белок волос, шерсти, ногтей, когтей, клюва, перьев и рогов, входящий также в состав кожи позвоночных. Твердость и растяжимость кератина варьируют в зависимости от числа дисульфидных мостиков между соседними полипептидными цепями (от степени сшивки цепей).
Теоретически все СО- и NH-группы могут участвовать в образовании водородных связей, так что α-спираль - это очень устойчивая, а потому и весьма распространенная конформация. Тем не менее большинство белков существует в глобулярной форме, в которой имеются также участки β-слоя и участки с нерегулярной структурой. Объясняется это тем, что образованию водородных связей препятствуют наличие некоторых аминокислотных остатков в полипептидной цепи, наличие дисульфидных мостиков между различными участками одной и той же цепи и, наконец, тот факт, что аминокислота пролин вообще неспособна образовывать водородные связи.
β-Слой, или складчатый слой, - это другой тип вторичной структуры. Белок шелка фиброин, выделяемый шелкоотделительными железами гусениц шелкопряда при завивке коконов, представлен целиком именно этой формой. Фиброин состоит из ряда полипептидных цепей, вытянутых сильнее, чем цепи с конформацией α-спирали. Эти цепи уложены параллельно, но соседние цепи по своему направлению противоположны одна другой (антипараллельны). Они соединены друг с другом при помощи водородных связей, возникающих между С=0- и NH-группами одной цепи и NH- и С=0-группами соседних цепей. В этом случае в образовании водородных связей также принимают участие все NH- и С=О-группы, т. е. структура тоже весьма стабильна. Такая конформация полипептидных цепей называется (β-конформацией, а структура в целом - складчатым слоем (рис. 5.35). Фиброин обладает высокой прочностью на разрыв и не поддается растяжению, но подобная организация полипептидных цепей делает шелк очень гибким. В глобулярных белках полипептидная цепь может складываться на себя, и тогда в этих точках глобулы возникают участки, имеющие структуру складчатого слоя.
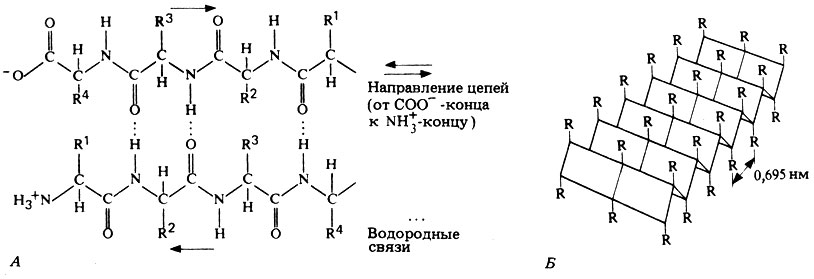
Рис. 5.35. Складчатый слой. Полипептидные цепи удерживаются рядом друг с другом при помощи водородных связей, образующихся между NH- и СО-группами. R-группы аминокислот располагаются над и под плоскостью этого складчатого слоя. А. Две антипараллельные полипептидные цепи. Б. Структура из трех полипептидных цепей изображена здесь так, чтобы показать складки между R-группами
Еще один способ организации полипептидных цепей мы находим у фибриллярного белка коллагена. Здесь три полипептидные цепи свиты вместе, образуя тройную спираль. В каждой полипептидной цепи этой сложной спирали, называемой тропоколлагеном (рис. 5.36), содержится около 1000 аминокислотных остатков. Такой белок тоже невозможно растянуть, и это его свойство существенно для той функции, которую он выполняет, например, в сухожилиях, костной и других видах соединительной ткани. Белки, существующие только в полностью спирализованной форме, подобно кератину или коллагену, представляют собой исключение среди прочих белков.

Рис. 5.36. Трехспиральная структура коллагена
Третичная структура
У большинства белков полипептидные цепи свернуты особым образом в компактную глобулу. Способ свертывания полипептидных цепей глобулярных белков называется третичной структурой. Третичная структура поддерживается уже обсуждавшимися выше связями трех типов - ионными, водородными и дисульфидными, а также гидрофобными взаимодействиями (рис. 5.37). В количественном отношении наиболее важны именно гидрофобные взаимодействия; белок при этом свертывается таким образом, чтобы его гидрофобные боковые цепи были скрыты внутри молекулы, т. е. защищены от соприкосновения с водой, а гидрофильные боковые цепи, наоборот, выставлены наружу.
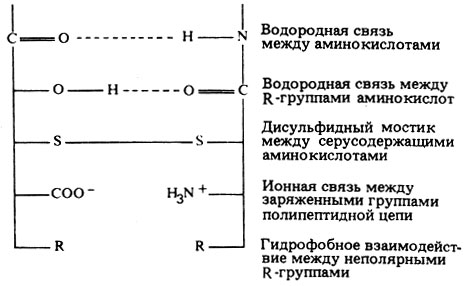
Рис. 5.37. Связи, стабилизирующие вторичную и третичную структуру белков. Особенно важны для поддержания структуры гидрофобные взаимодействия (объединения неполярных молекул или отдельных частей молекул), позволяющие исключить молекулы воды, что очень существенно, например, для мембран, учитывая водное окружение клетки
Для определения третичной структуры белков можно использовать метод рентгеноструктурного анализа. К началу 1963 г. Кендрью и Перуц (Kendrew, Perutz) определили этим методом вторичную и третичную структуру миоглобина (рис. 5.38). Теперь для миоглобина были известны:

Рис. 5.38. А. Первичная структура миоглобина.
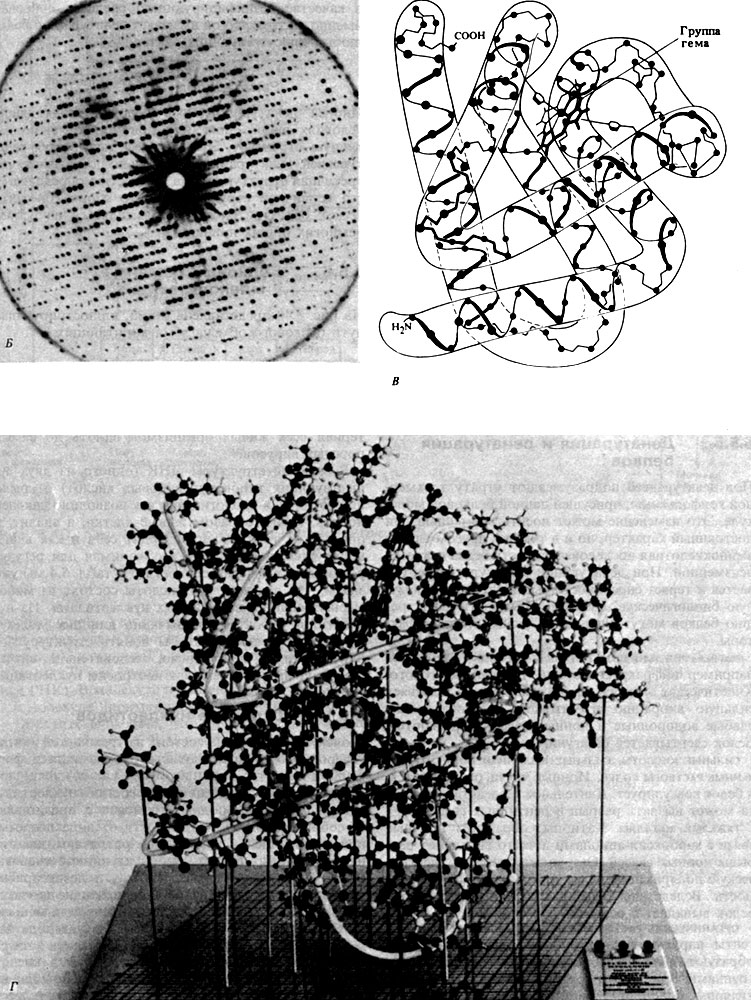
Рис. 5.38. Б. Рентгенограмма миоглобина (из мышц кашалота). Регулярное расположение пятен есть результат рассеяния (дифракции) падающего на фотопленку рентгеновского излучения вследствие его взаимодействия с атомами миоглобина в кристалле. Фотография - это двумерное сечение трехмерного расположения дифракционных пятен. По распределению и интенсивности дифракционных пятен определяют положение отдельных атомов в молекуле. (По J. С. Kendrew, Scientific American, December 1961.) В. Конформация миоглобина, установленная на основе рентгеноструктурного анализа с высоким разрешением. Г. Модель миоглобина
Первичная структура - молекула представляет собой одну полипептидную цепь, построенную из 153 аминокислотных остатков (их последовательность была установлена в начале 60-х годов);
Вторичная структура - около 75% цепи имеет α-спиральную конформацию (восемь спиральных участков);
Третичная структура - α-спираль свернута нерегулярным образом в компактную глобулу;
Простетическая группа - гемогруппа, или гем (содержит железо).
Сведения о функции миоглобина читатель найдет в гл. 14.
Четвертичная структура
Многие белки с особо сложным строением состоят из нескольких полипептидных цепей, удерживаемых в молекуле вместе за счет гидрофобных взаимодействий, а также при помощи водородных и ионных связей. Способ совместной упаковки и укладки этих полипептидных цепей называют четвертичной структурой белка. Четвертичная структура имеется, например, у гемоглобина. Его молекула состоит из четырех отдельных полипептидных цепей двух разных типов: из двух α-цепей и двух β-цепей. Две α-цепи содержат по 141 аминокислотному остатку, а две (β-цепи-по 146 остатков. Полную структуру гемоглобина определили Кендрью и Перуц (Kendrew, Perutz). В схематическом виде она представлена на рис. 5.39.

Рис. 5.39. Структура гемоглобина. Молекула состоит из четырех полипептидных цепей: двух α-цепей и двух β-цепей. С каждой цепью связана одна группа тема, к которой присоединяется молекула кислорода. Гемоглобин - пример белка, состоящего из отдельных субъединиц, т. е. обладающего четвертичной структурой
Некоторые вирусы, например вирус мозаики табака, имеют белковую оболочку, состоящую из многих полипептидных цепей, упакованных высокоупорядоченным образом (рис. 2.15).
На страничках портала подобраны анкеты с персональными фотографиями и видосами шлюх. В свою очередь шлюхи Астрахани поведали подробно перечень своих эротических умений. Снимите одну из них прямо сейчас!
|
ПОИСК:
|
При копировании ссылка обязательна:
http://biologylib.ru/ 'Библиотека по биологии'