
Сверхновая звезда
Возраст нашей Галактики, Млечного Пути, составляет 10-15 миллиардов лет. Она имеет форму утолщенного в центре диска, где находятся миллиарды больших звезд. Когда одна из этих звезд гибнет, при взрыве ее высвобождаются частицы, обладающие достаточной энергией, чтобы достичь удаленных частей спиральных рукавов Галактики. Энергия этих частиц достаточна также для того, чтобы вступать в ядерные реакции, необходимые для образования всех элементов периодической системы.
Почему, однако, во время гибели звезды должен происходить взрыв? Звезда состоит в основном из газообразного водорода. При старении под влиянием гравитационных сил происходит ее сжатие. При таком сжатии плотность увеличивается. Возрастание плотности ускоряет процесс сжатия, и этот процесс происходит до тех пор, пока плотность ядра звезды не достигнет плотности ядерного вещества. На этой критической стадии быстро развиваются огромные силы отталкивания, и ядро взрывается.
Выброшенное при взрыве вещество представляет собой космический газ и пыль, которые, вероятно, содержат все элементы периодической системы, но в основном все еще водород (около 90%). Кроме водорода в них присутствуют гелий, прочие инертные газы и метан. Другие элементы входят в состав частиц пыли, образующейся при взрыве, и составляют лишь несколько тысячных процента от всей массы газа и пыли. Однако количество выбрасываемого при взрыве сверхновой звезды вещества столь велико, что даже эта ничтожная доля достаточна для образования Солнца и планет Солнечной системы.
Вспышка сверхновой звезды, которая дала материал для нашей Солнечной системы, произошла более 5 млрд. лет назад. Подобную вспышку люди наблюдали в 1054 г. Вначале она была настолько яркой, что ее можно было видеть среди белого дня невооруженным глазом. С тех пор большая часть выброшенного вещества рассеялась в космосе, однако остаток этой сверхновой все еще виден ночью в телескоп. Это светящееся облако газа и пыли называется Крабовидной туманностью (рис. 1.1). Вспышку сверхновой звезды наблюдали в 1054 г. японские и китайские астрономы. В настоящее время известно, что Крабовидная туманность находится на расстоянии 6000 световых лет от Земли, т. е. вспышка произошла за 6000 лет до того, как она предстала глазам ученых Востока, которые отметили, что "звезда-гостья" ярче Венеры. Эту сверхновую можно было наблюдать невооруженным глазом более года. Затем она постепенно рассеялась в космическом пространстве. Светимость сверхновой может в 100 млн. раз превышать светимость нашего Солнца. Особенность Крабовидной туманности состоит в том, что она испускает не только видимое (сейчас уже не очень яркое), но также рентгеновское и радиоизлучение. Источником радиоволн является пульсар, представляющий собой быстро вращающуюся очень плотную звезду. Пульсар Крабовидной туманности - это единственный известный в настоящее время пульcap, который можно видеть в оптический телескоп.
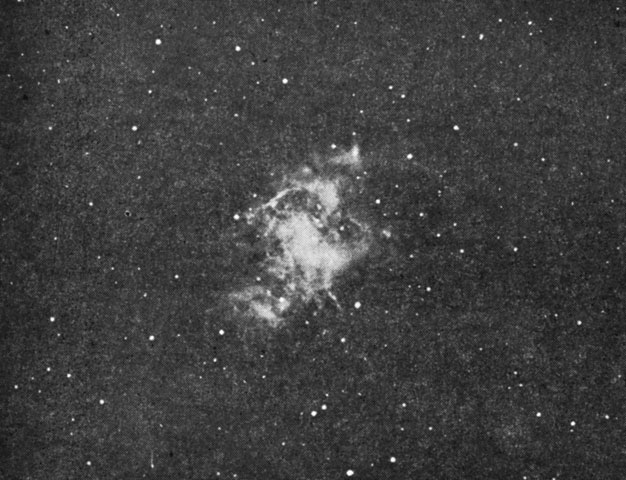
Рис. 1.1. Крабовидная туманность, представляющая собой остатки взрыва сверхновой звезды
Часть космического газа и пыли, выброшенная при взрыве сверхновой, тогда же, примерно 5 млрд. лет назад, достигла места нынешнего расположения нашей Солнечной системы - периферии Галактики, где она уплотнилась, образовав диффузное облако. И в этом случае силы самогравитации привели к уплотнению внутренней, более плотной части облака, в результате чего появилась другая звезда, но меньшего размера - наше Солнце.
Остаток космического вещества удерживался за счет гравитационного притяжения Солнца и постепенно слипался, образовав Землю и другие планеты. Масса Земли была недостаточной, чтобы удержать космический газ, и большая его часть рассеялась в космосе. Сначала Земля представляла собой просто скопление космической пыли, довольно холодное, и почти не имела атмосферы. Так обстояло дело 4,8 млрд. лет назад.
Облако космической пыли - юная Земля - состояло из металлов и их окислов, воды в виде льда и в виде гидратов, аммонийных кремневых и сернистых соединений и карбидов. Это облако все более уплотнялось за счет собственной гравитации, а огромное давление, вызываемое этим уплотнением, особенно в центре, привело к повышению температуры уплотняющейся массы. Химические реакции, начавшиеся в результате повышения температуры, усилили разогрев, и постепенно Земля разделилась на плотное расплавленное ядро, мантию и кору. Летучие вещества и газы под воздействием тепла переместились к поверхности. Эти молекулы образовали первоначальную атмосферу Земли. Атмосфера состояла тогда не из азота и кислорода, как в наши дни. Она содержала метан, аммиак и пары воды до тех пор, пока земная кора не остыла настолько, что смогли образоваться первичные океаны.
Земля тех времен представляла собой океан и безжизненные скалы, раскаляемые сиянием молодого Солнца. Поскольку излучение Солнца не фильтровалось слоем озона, который имеется в атмосфере в наши дни, оно состояло в основном из ультрафиолетовых лучей (УФ-лучи), обладающих высокой энергией, которая нужна для того, чтобы превращать простые молекулы первоначальной атмосферы в новые молекулы, способные к дальнейшим реакциям образования сложных молекул жизни. Двумя наиболее важными из этих новых молекул являются формальдегид и цианистый водород, образующиеся посредством фотолиза. Формальдегид образуется из метана и воды под действием УФ-излучения.
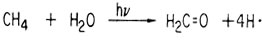
Эта реакция включает следующие стадии:
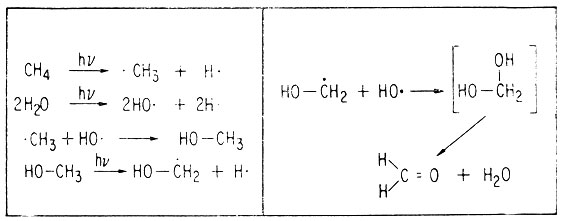
Цианистый водород образуется под действием УФ-излучения из метана и аммиака. Эта реакция включает такие же стадии.
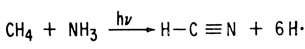
Синтез формальдегида и цианистого водорода в первичном безжизненном океане дает ключ к разгадке тайны появления двух основных составляющих жизни - белков и нуклеиновых кислот.
Молекула белка представляет собой длинную цепь, состоящую из аминокислот, соединенных друг с другом по типу "голова-хвост". Простейшей аминокислотой является глицин
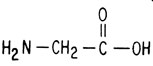
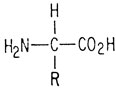
В белок может входить до 20 различных аминокислот. Все они имеют такое же строение, как и глицин, и отличаются только боковыми цепями. В приведенной ниже общей формуле R обозначает одну из 20 боковых цепей - 20 различных аминокислот служат строительным материалом для создания всего многообразия белковых молекул:
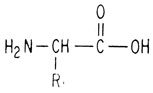
Если R=H, аминокислота называется глицином. Если R=CH3, аминокислота называется аланином. Если "голова" (имеется в виду конец молекулы, несущий карбоксильную группу) одной аминокислоты присоединяется к "хвосту" (конец молекулы, несущий аминогруппу) другой аминокислоты, выделяется молекула воды и образуется амидная или пептидная связь.
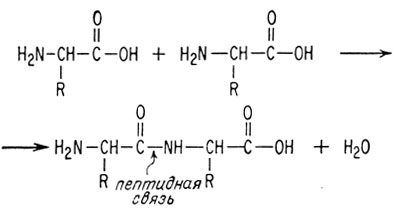
Вот почему белок называют полипептидом. Часть молекулы белка изображена ниже
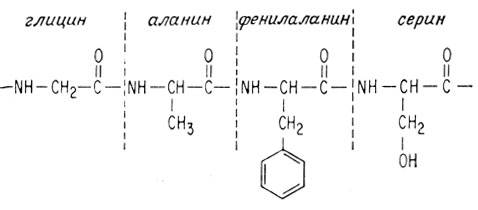
Однако как в первичном океане из формальдегида, цианистого водорода, аммиака и воды могла образоваться аминокислота? Возможный путь получения глицина включает всего три стадии*.
* (Об аминонтириле еще будет сказано дальше.)
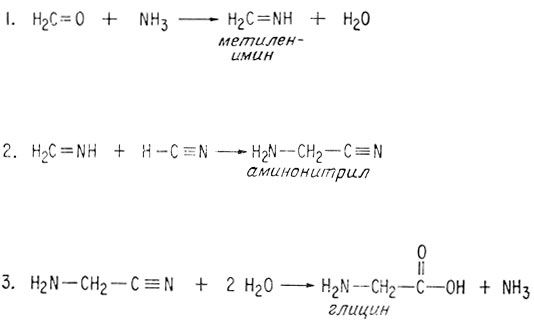
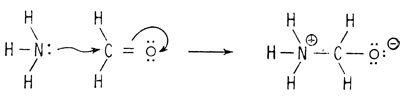
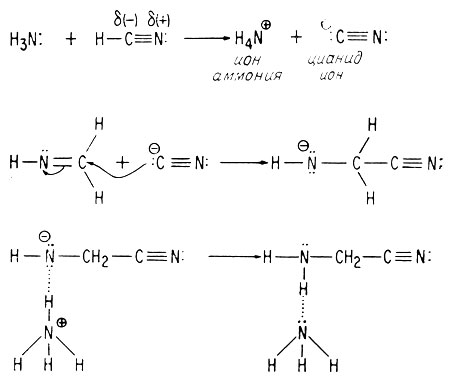
Первая стадия начинается нуклеофильной атакой карбонильной группы формальдегида аммиаком.
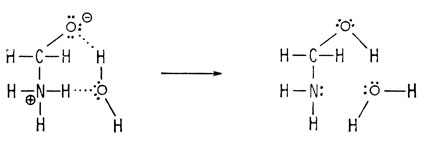
Заряд нейтрализуется за счет переноса протона, возможно, происходящего с помощью молекулы воды.
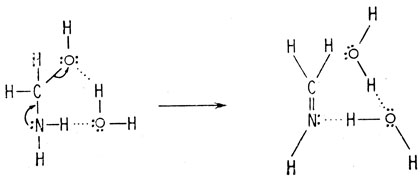
Затем за счет переноса протона из нестабильного гидрата образуется имин.
Вторая стадия требует нуклеофильной атаки углеродного атома имина ионом цианида. Углерод в ионе цианида является более отрицательно заряженным концом иона и поэтому более сильным нуклеофилом, чем азот.
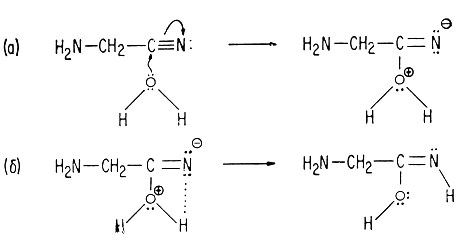
Третьей и последней стадией синтеза глицина является гидролиз образовавшегося аминонитрила, приводящий к получению аминокислоты. Эта стадия также включает нуклеофильную атаку, но на этот раз нуклеофильным агентом является вода. В приведенных ниже реакциях реакция (а) изображает нуклеофильную атаку молекулой воды, реакция (б) - перенос протона.
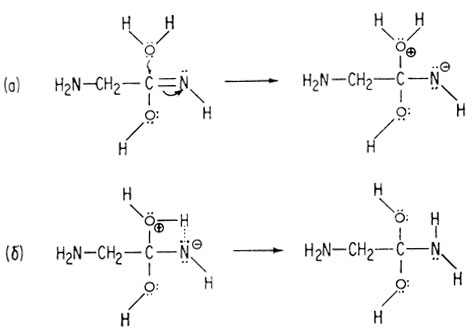
Появляющийся при этом атом углерода, связанный двойной связью с атомом азота, также открыт для нуклеофильной атаки, поэтому эта стадия повторяется.
Образующийся двухатомный аминоспирт нестабилен и может распадаться, выделяя либо молекулу воды, либо молекулу аммиака. Если при распаде выделяется вода, он просто превращается в иминоспирт, из которого он был получен. Этот иминоспирт является менее стабильной формой глицинамида. Однако обе формы подвержены нуклеофильной атаке.
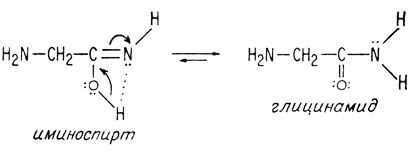
Если при распаде двухатомного аминоспирта выделяется аммиак, продуктом является глицин.
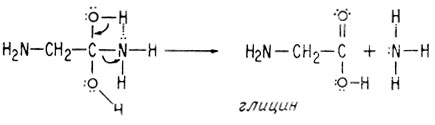
Соединение этих звеньев с образованием полипептидных цепей могло происходить в первичном океане на стадии аминонитрила, т. е. до гидролиза нитрила, приводящего к образованию карбоновой кислоты. Действительно, это могло быть самым простым способом образования первичных полипептидов, поскольку гидролиз, нитрила и конденсация аминокислоты требуют довольно жестких или же специальных условий проведения реакции. Аминонитрилы могли бы полимеризоваться и гидролизоваться в более мягких условиях, по сравнению с имевшимися в то время.
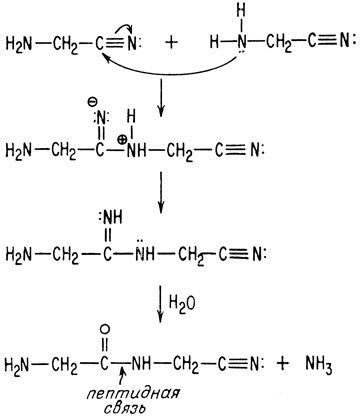
Вероятный путь добиологического образования пептидов
Стадия гидролиза аналогична равновесию имин - альдегид. Каждый из концов молекулы, образовавшейся при соединении двух молекул, еще содержит реакционноспособную группу, что позволяет бесконечно наращивать цепь.
Для проверки гипотезы о самопроизвольном возникновении аминокислот и других молекул жизни в условиях, которые, как считают, должны были существовать в первичной атмосфере Земли и океана, были проведены лабораторные опыты. В 1953 г. в Чикагском университете Стенли Миллер подвергал в течение недели действию электрического разряда смесь метана, аммиака, воды и водорода. В конце опыта при гидролизе реакционной смеси он обнаружил глицин и другие аминокислоты. Действительно, более 2% метана исходной смеси превратились в глицин. Этот замечательный результат ясно показывает, что в природе по крайней мере при определенных условиях проведения реакции происходит образование молекул жизни, и в гораздо большей степени, чем можно было бы ожидать по соображениям статистики. Как этот, так и другие эксперименты, проведенные позже, показывают, что аминокислоты и другие важные для жизни молекулы могли образоваться небиогенным путем. Однако было ли так на самом деле? Есть ли в природе свидетельства того, что когда-либо это случилось на Земле или где-либо еще во Вселенной? Да, есть!
В 1970 г. другой ученый, также занимающийся происхождением молекул жизни, обнаружил аминокислоты в метеорите, упавшем в Австралии. Шесть из этих аминокислот аналогичны аминокислотам, обнаруживаемым в живой материи, существующей на Земле. Это открытие говорит о том, что либо аминокислоты действительно образовались где-то во Вселенной абиогенным путем, либо существует внеземная жизнь. Без сомнения, открытие существования внеземных аминокислот не опровергает ни одну из этих возможностей. Обе могут быть справедливы. По крайней мере хотя бы одна из них должна быть верна.
Если верно первое предположение, тогда получен ответ на поставленный ранее вопрос. Аминокислоты действительно могли образоваться в природе абиогенным путем. Ученые полагают, что открытие внеземных аминокислот подтверждает первое предположение, поскольку они оптически неактивны, т. е. они не вращают плоскость поляризации света. Аминокислоты же биологического происхождения оптически активны. Для аминокислот, выделенных из живущих на Земле организмов, всегда наблюдалась оптическая активность и предполагается, что это должно быть справедливо для всей Вселенной. Аминокислоты, синтезированные небиогенным путем в опытах, имитирующих первичную атмосферу Земли, не обладают оптической активностью.
Почему аминокислоты могут быть оптически активными в одном случае и оптически неактивными - в другом? Каждая молекула аминокислоты содержит атом углерода, связанный с четырьмя различными атомами или группами.
Поскольку этот атом углерода лежит в центре тетраэдра, молекула может иметь две конфигурации (т. е. возможны два способа расположения атомов в пространстве).
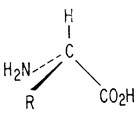
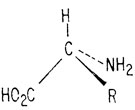
Такие две молекулы относятся друг к Другу так же, как левая и правая рука - они очень похожи, но не одинаковы. Их нельзя наложить друг на друга так, чтобы каждый атом совместился с аналогичным ему атомом. В то же время молекулы эти настолько сходны, что имеют одинаковые физические свойства, за исключением того, что одна из них вращает плоскость поляризации света по часовой стрелке, а другая - против часовой стрелки. Поэтому их называют энантиомерами, или, что менее удобно, оптическими антиподами*. Их называют также стереоизомерами для того, чтобы показать, что они различаются только пространственным расположением атомов. Порядком расположения атомов, как геометрические изомеры, они не отличаются.
* (Об энантиомерах, или оптических антиподах, см. приложение.)
Атом углерода, соединенный с четырьмя различными заместителями, называют асимметрическим атомом. Присутствие в молекуле такого атома делает всю молекулу в целом несимметричной, т. е. способной образовывать несовмещаемые, зеркальные изображения - энантиомеры.
Если аминокислота представляет собой смесь равных количеств обоих энантиомеров, то она оптически неактивна. Такая смесь называется рацемической. Рацемическая смесь не вращает плоскость поляризации света, потому что вращение, производимое одним энантиомером, компенсирует вращение другого энантиомера.
Всякая аминокислота, выделенная из белков, напротив, состоит только из одного из двух возможных энантиомеров. Поэтому она вращает плоскость поляризации света или по часовой стрелке, или против часовой стрелки, т. е. является лево-, либо правовращающей. Однако независимо от направления вращения плоскости поляризации света и от того, с какой аминокислотой мы имеем дело, ориентация заместителей относительно асимметрического углеродного атома всегда одинакова. Эту ориентацию или конфигурацию называют L-конфигурацией, когда при превращении такой аминокислоты в глицериновый альдегид без изменения ее конфигурации получается левовращающий глицериновый альдегид. Энантиомеры аминокислот белков обозначают буквой о, если из них получается правовращающий глицериновый альдегид.
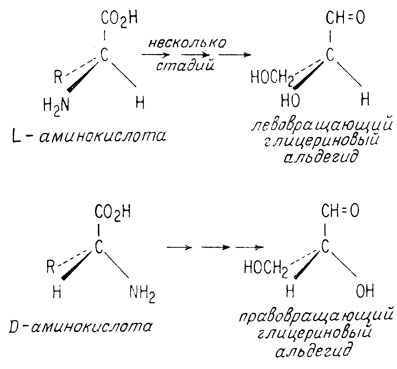
Антиподы глицеринового альдегида были обозначены произвольно, еще до разработки способов определения пространственной структуры. Позже правильность такого обозначения была подтверждена посредством рентгенографии (гл. 11).
Все аминокислоты, выделяемые из белков, всегда имеют L-конфигурацию независимо от того, являются ли они лево- или правовращающими, поскольку по стереохимическому строению они связаны с L-глицериновым альдегидом. Лево- и правовращение обозначают маленькими буквами l и d или символами - и +.
Трудно объяснить, почему в белках присутствуют только L-аминокислоты. Но нетрудно объяснить существование полностью L-белка или даже полностью L-организма, а не смешанного L- И D -белка или организма. К этому мог привести естественный отбор, поскольку полностью L-форма энергетически неэквивалентна смеси L- и D-форм. Возможно, полностью L-белок работает гораздо лучше, чем смешанный L- и D-белок. Однако полностью D-белок или полностью D-организм был бы абсолютно эквивалентен своему зеркальному L-близнецу. Поэтому параллельно самопроизвольному зарождению и развитию L-ЖИЗНИ должна была бы возникнуть и развиваться D-жизнь. Однако этого не произошло, и современная наука не может объяснить почему.
Другой всегда наблюдаемый факт - образование оптически неактивных продуктов из оптически неактивных веществ. Так например, если синтезировать аминокислоту аланин в лаборатории из ацетальдегида, аммиака, цианистого водорода и воды, получится рацемическая смесь энантиомеров.
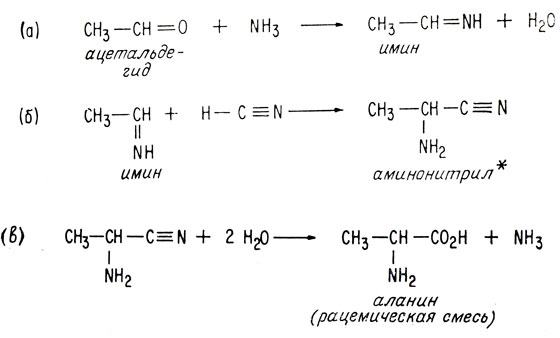
* (См. формулу этого соединения, приведенную выше.)
Основной причиной образования обоих стереоизомеров аланина является равновероятность подхода иона цианида во время атаки с любой стороны плоскости молекулы имина.
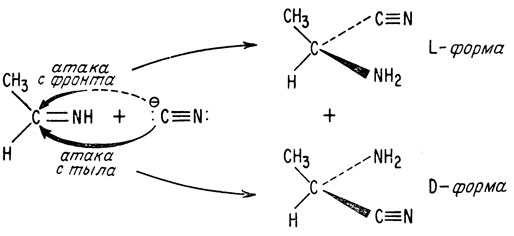
Однако, когда аланин синтезируется в живом организме, реакция происходит на поверхности асимметрического катализатора? называемого ферментом. Если сам фермент всегда присоединяется к имину с фронта, атака ионом цианида может осуществляться только с тыла. При этом будет образовываться лишь один из двух антиподов аланина. Такая модель стереоспецифичного действия ферментов отвечает наблюдаемому в процессе биосинтеза образованию одного только вида энантиомеров.
|
ПОИСК:
|
© BIOLOGYLIB.RU, 2001-2020
При копировании ссылка обязательна:
http://biologylib.ru/ 'Библиотека по биологии'
При копировании ссылка обязательна:
http://biologylib.ru/ 'Библиотека по биологии'