
6. Могущественные молекулы
Убийцы микробов
Как мы видели в гл. 5, человек накопил достаточный арсенал средств, защищающих его от боли и физических страданий. Обратимся теперь к проблеме болезней и к тому, как человек использовал чудесные молекулы, созданные природой, а затем сам создал большое число специфических молекул, помогающих отражать нашествие микробов.
Во времена, предшествовавшие открытию хинина, т. е. примерно 300 лет назад, возбудители ужасной перемежающейся лихорадки- малярии - беспрепятственно развивались в крови человека. Даже в тех странах и городах, которые, казалось бы, совсем не подходили по климату для распространения этой болезни, например в Риме и Лондоне, малярия уносила много человеческих жизней. Переносчики этой болезни - зараженные плазмодиями комары Anopheles. В организме этих комаров плазмодии быстро размножаются. При укусе такого комара плазмодии со слюной комара попадают в кровь человека, а оттуда - в печень. В печени они размножаются, а затем проникают в эритроциты.
Хинин оказал почти невероятное лечебное действие на больных малярией, испытывавших изнурительные страдания, а зачастую и умиравших. Он нанес также сокрушительный удар по учению Галена - лжемедицинскому учению, в течение 1500 лет владевшему умами врачей и господствовавшему во врачебной практике, - с его слабительными и кровопусканиями. Хинин - это замечательная молекула, имеющая увлекательную историю.
В свете этой истории кажется совершенно недопустимым, что малярия в последнее десятилетие все еще угрожает трети населения земного шара. Ежегодно от малярии умирает около 2 млн. человек, а число больных, страдающих хронической малярией, составляет сотни миллионов.
Способность хинина излечивать малярию связана со структурой его молекулы. Как же выглядит эта молекула?
Молекула хинина состоит из хинолиновой и хинуклидиновой частей, соединенных друг с другом спиртовым углеродным атомом (карбинольный мостик).
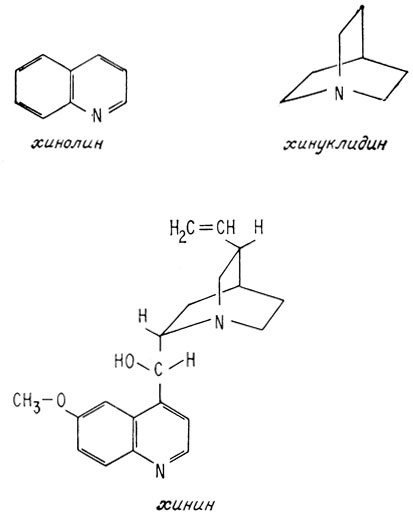
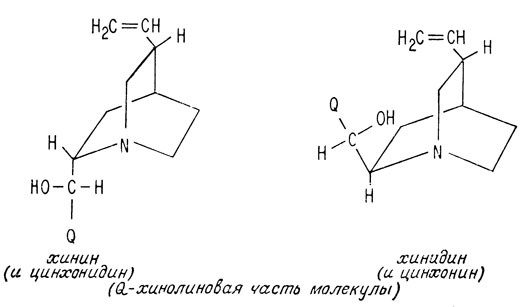
Хинин вырабатывается хинным деревом, родиной которого является Перу, и находится в коре этого дерева. Каким образом хинное дерево вырабатывает хинин - неизвестно. В коре его содержатся еще три алкалоида, по строению очень похожие на хинин, - хинидин, цинхонин и цинхонидин, которые также активны против возбудителей малярии. Своей исключительной популярностью хинин обязан лишь случайности - он был выделен первым из этих четырех алкалоидов. Хинин и хинидин отличаются конфигурацией асимметрического атома углерода хинуклидиновой части, присоединенного к карбинольному мостику. Цинхонидин и цинхонин не имеют метоксигруппы (CH3O-) в хинолиновой части молекулы.
Как были открыты лечебные противомалярийные свойства коры хинного дерева - неизвестно. Существует много версий, касающихся того, как было сделано это открытие. Одна из них приписывает его священнику-иезуиту, который жевал кору различных деревьев для того, чтобы по вкусу отличать разные ботанические виды. Другая версия приписывает это открытие корабельному хирургу, который наблюдал, как горные львы, у которых была лихорадка, искали хинное дерево и жевали его кору. Третья версия утверждает, что страдавший малярией больной, внезапно сраженный приступом лихорадки и мучимый жаждой, в отчаянии напился из водоема, вода в котором была горькой от хинного дерева, поваленного в него недавней бурей, - и выздоровел.
Еще больше запутывает и без того неясное происхождение этого способа лечения следующее обстоятельство: некоторые историки полагают, что южноамериканские индейцы знали о противомалярийных свойствах коры хинного дерева задолго до открытия Нового Света, но скрыли это от европейцев в надежде на то, что болезнь уничтожит непрошенных чужеземцев. Другие, однако, утверждают, что индейцы не знали о лечебных свойствах коры, да и не нуждались в этом, поскольку малярия в Новый Свет была завезена европейцами.
Как бы то ни было, первое письменное сообщение о замечательном действии этого средства появилось в 1633 г. в Хронике Святого Августина, написанной отцом Каланча в Южной Америке. Он писал, что дерево, называемое хинным, имеет кору цвета корицы, которая, если ее измельчить в порошок и приготовить из этого порошка напиток, вылечивает лихорадку. Как ни странно, это сообщение не привело немедленно к экспорту коры хинного дерева в Европу, несмотря на большое число больных малярией.
Прошло еще двенадцать долгих лет, прежде чем, как рассказывает история, отец Тафур привез немного коры хинного дерева на церковный собор в Рим, жители которого тогда повально болели малярией. Успехи, достигнутые при лечении, вскоре побудили священников-иезуитов в Южной Америке начать отправку коры хинного дерева в Рим, где она стала называться "корой иезуитов". Паломники, посещавшие Рим, получали пакетики порошка, облегчавшего их страдания. Таким путем весть о новом лекарстве быстро разнеслась по всей Европе. Несмотря на популярность коры хинного дерева, врачи, воспитанные на учении Галена, не хотели и слышать о настое иезуитов. Согласно учению Галена, греческого врача, практиковавшего в Риме во втором веке, болезни происходят от нарушения равновесия между четырьмя началами в организме, а именно кровью, слизью, черной желчью и желтой желчью. Лечение, которое Гален рекомендовал при лихорадке, возникавшей, по его представлениям, в результате нарушения равновесия между черной и желтой желчью, состояло в кровопускании или приеме слабительных или комбинации того и другого. Влияние Галена, очень широко распространенное благодаря тому, что им было написано более 500 книг, задержало развитие медицины примерно на 1500 лет вплоть до открытия "коры иезуитов". Конклав, состоявшийся в Риме в 1655 г., впервые в истории римской церкви прошел без смертей его участников от малярии. Распространению и более широкому применению спасительного порошка препятствовали также религиозные противоречия. В протестантских странах применение этого лекарства не разрешалось. В то время, когда проходил римский конклав, во время которого не умер ни один из участников, в Лондоне малярия продолжала косить население. Оливер Кромвель, ярый сторонник протестанства, был болен малярией, но он и слышать не хотел о том, чтобы попробовать это запрещенное средство, и умер от малярии в 1658 г.
Еще через двенадцать лет те лондонские богачи, которые могли позволить себе заплатить высокую цену, получили возможность вылечиться от малярии у некоего Роберта Тальбора, в недавнем прошлом безвестного, но предприимчивого помощника аптекаря. Хитрый Тальбор публично предупреждал об опасностях, связанных с применением коварного порошка иезуитов, а сам готовил и продавал его под видом своего собственного нового секретного лекарства. Однако его популярность скоро восстановила против него коллег из Королевского медицинского колледжа, поскольку он не пускал кровь и не применял слабительные. Выдвинутые против Тальбора обвинения в антигаленизме были вскоре сняты и вот почему. Король Карл 11 заболел малярией и обратился к Тальбору, который его вылечил. За это Тальбор был возведен в рыцари и ему было пожаловано звание королевского врача. После смерти Тальбора секрет его препарата был раскрыт, и постепенно кора из Перу получила признание.
Следующим достижением в борьбе человека против малярии явилось выделение в 1820 г. двумя французскими фармакологами Жозефом Пеллетье и Жозефом Кавенту хинина из коры хинного дерева. Они не запатентовали свой метод, а просто дали возможность промышленникам изготавливать и продавать чистый хинин, что впервые дало миру мощное противомалярийное средство в необходимых количествах.
Первые попытки установить структуру молекулы хинина относятся к 1854 г., когда А. Стрекер выяснил его формулу C20H24N2O2. В конце прошлого века была получена и другая важная информация относительно структуры этой молекулы, хотя полностью ее строение не было известно. Было установлено, что оба атома азота являются третичными (R3N:), поскольку каждый из них способен реагировать с молекулой йодистого этила, образуя четвертичную соль аммония. Таким образом, молекула не содержит групп N-H
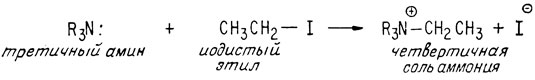
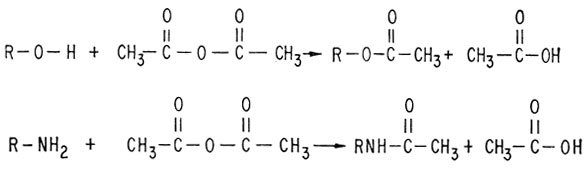
Поскольку при действии уксусного ангидрида образуется ацетилпроизводное, один из атомов кислорода должен входить в группу O-H - единственную способную ацетилироваться группу, которую можно составить из атомов, имеющихся в хинине.
Наличие двойной связи было доказано путем получения продуктов присоединения (галогеноводородных кислот и брома)
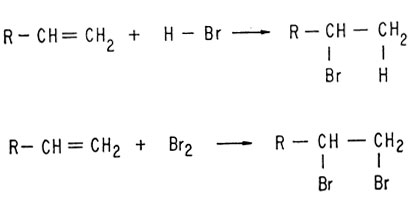
Установлено, что эта двойная связь - винильного типа (-CH=CH2), поскольку при окислении образуются две карбоновые кислоты, одна из которых является муравьиной:
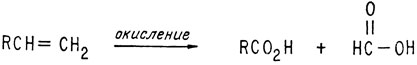
Таким образом, было известно, что молекула хинина содержит две третичные аминогруппы, спиртовую группу и винильную двойную связь.
Первая важная информация об основном скелете молекулы появилась в 1883 г., когда было показано, что при сплавлении хинина со щелочью образуется 6-метоксипроизводное хинолина
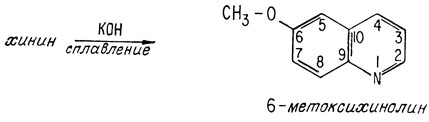
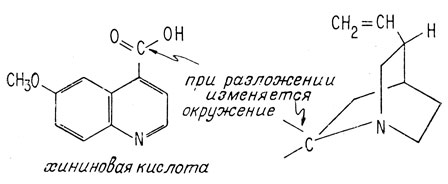
После того как установили, что окисленный фрагмент молекулы хинина имеет карбоксильную группу в положении 4, было высказано предположение, что, вероятно, этот фрагмент присоединен к остальной молекуле также в положении 4. Этот фрагмент был назван хининовой кислотой
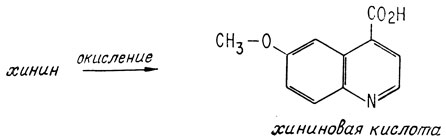
Хининовая кислота содержит 11 атомов углерода. Остальные 9 углеродных атомов хинина входят в другой фрагмент, получаемый при его разложении и называемый мерохиненом. Он был получен при разложении ангидрохинина под действием фосфорной кислоты
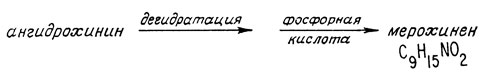
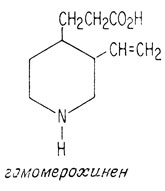
При помощи сложного ряда превращений родственных соединений в конце прошлого века было показано, что мерохинен представляет собой пиперидин, в котором в положении 3 имеется винильная группа, а в положении 4 - остаток уксусной кислоты
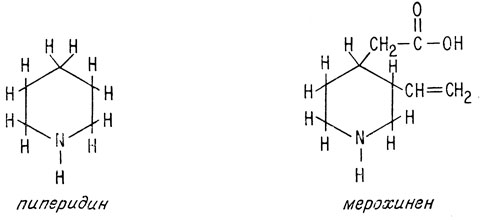
Рассмотрение различных атомов, входящих в молекулу мерохинена, с учетом того, что уже известно о молекуле хинина в целом, приводит к выводу, что в процессе разрушения молекулы атом углерода, входящий в карбоксильную группу, и атом азота изменяются. На это указывает тот факт, что в хинине нет ни карбоксильной группы, ни группы N-H. Простейшим способом воссоздания структуры молекулы является, таким образом, образование связи между углеродом карбоксильной группы и атомом азота. При этом образуется хинуклидиновая часть молекулы.
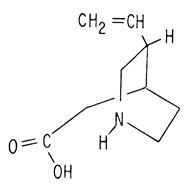
Мерохинен
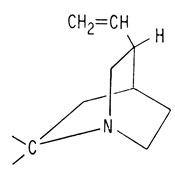
Возможная структура фрагмента хинина
Так как при действии фосфорной кислоты никакие другие атомы этого фрагмента, состоящего из 9 углеродных атомов, не затрагиваются, местом, которым этот фрагмент присоединяется к остальной молекуле, является также углерод карбоксильной группы.
Из 11 атомов углерода, которые, как было показано ранее, входят во фрагмент, называемый хининовой кислотой, один атом углерода карбоксильный. Очевидно, этот атом также появляется уже при разложении молекулы, поскольку хинин не содержит карбоксильной группы. Таким образом, напрашивается наиболее простой путь воссоздания молекулы хинина в целом - соединение этих атомов друг с другом.
В подобной структуре имеются все атомы, входящие в молекулу хинина, кроме одного атома кислорода, который, как известно, входит в гидроксильную группу. Гидроксильная группа, вероятно,
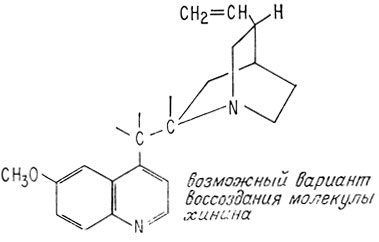
может находиться у любого из реакционноспособных атомов углерода. Если бы она находилась у углеродного атома хининовой кислоты, это была бы вторичная гидроксильная группа (R2CH-OH), которая должна была бы окисляться непосредственно до кетона
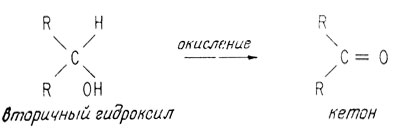
Возможен также и такой вариант, что гидроксильная группа присоединена к атому углерода, связанному с атомом азота. Учитывая стабильность молекулы, это гораздо менее вероятно. Во всяком случае, при такой структуре прямое образование кетона без разрушения скелета молекулы было бы невозможным. В 1907 г. было осуществлено прямое получение кетона, показавшее, что гидроксильная группа действительно является вторичной.
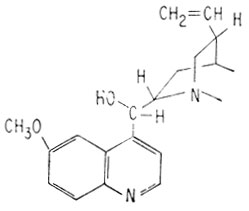
Угрожающий дефицит хинина в годы второй мировой войны ускорил осуществление полного синтеза этой предполагаемой структуры, который окончательно подтвердил бы ее справедливость и дал бы ответ на некоторые нерешенные вопросы стереохимии молекулы. Синтез хинина был блестяще осуществлен Р. Вудвордом и В. Дёрингом; сообщение об этом было опубликовано в 1945 г. Однако молекула является настолько сложной, что, вероятно, никогда на практике источником хинина не станет полный его синтез. Кроме того, одновременно была успешно осуществлена интенсивная программа разработки более простых синтетических противомалярийных средств, которая дала в руки союзников средство борьбы с этой изнуряющей болезнью.
Тем не менее синтез хинина остается поистине классическим примером органического синтеза. Как отмечали Вудворд и Дёринг в статье, посвященной синтезу хинина, опубликованной в журнале Американского химического общества, они использовали при синтезе хинина проведенные ранее другими исследователями работы, вершиной которых явился синтез дигидрохинина, осуществленный за 15 лет до этого.
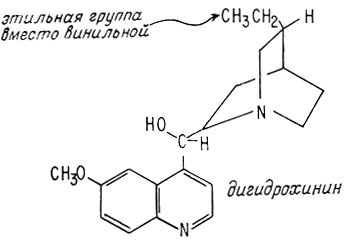
Полный синтез дигидрохинина был осуществлен благодаря получению и разделению стереоизомеров дигидрогомомерохинена. Это было сделано немецким химиком Рейбом, впервые предложившим правильную структуру хинина в 1908 г.
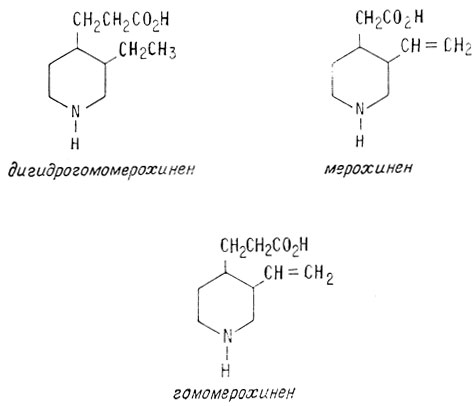
Остальная часть работы была уже выполнена. Хининовая кислота была синтезирована в 1912 г. независимо двумя группами исследователей. Рейб уже показал, что дигидрогомомерохинен (полученный из природных источников) может присоединяться к эфирам хининовой кислоты, в результате чего образуется дигидрохинотоксин.
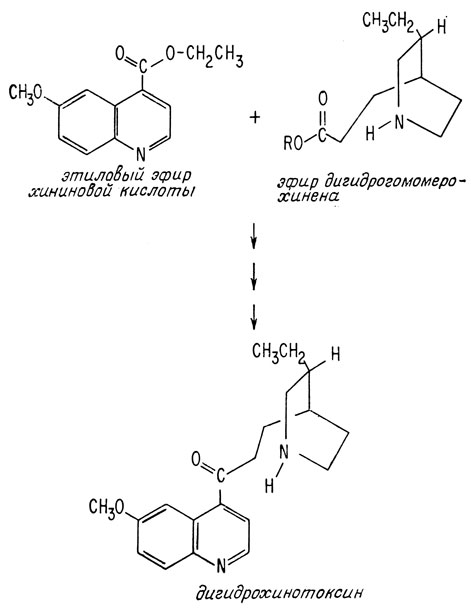
Сам хинотоксин был впервые получен из хинина Пастером еще в 1853 г. В 1918 г. Рейбу удалось превратить природный хинотоксин опять в хинин. Таким образом, единственным недостающим звеном полного синтеза дигидрохинина был синтез дигидрогомомерохинена. В 1931 г. Рейб осуществил этот синтез, исходя из β-коллидина, впервые синтезированного за 10 лет до этого.
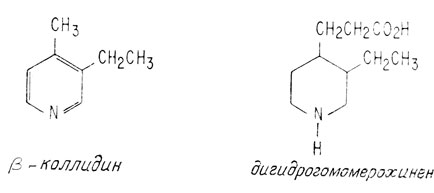
Учитывая результаты всех этих работ, Вудворд и Дёринг рассудили, что переход к хинину можно будет легко осуществить, если получить гомомерохинен. Поэтому они направили свои усилия на синтез этого вещества.
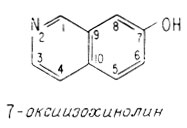
В качестве исходного соединения они выбрали 7-оксиизохинолин, поскольку эта молекула содержит почти полный азот-углеродный скелет гомомерохинена и синтез ее уже был осуществлен Фритчем в 1895 г.
Не вдаваясь во множество трудностей и осложнений, сопровождающих превращение 7-оксиизохинолина в гомомерохинен, сокращенно схема этого синтеза приведена ниже:
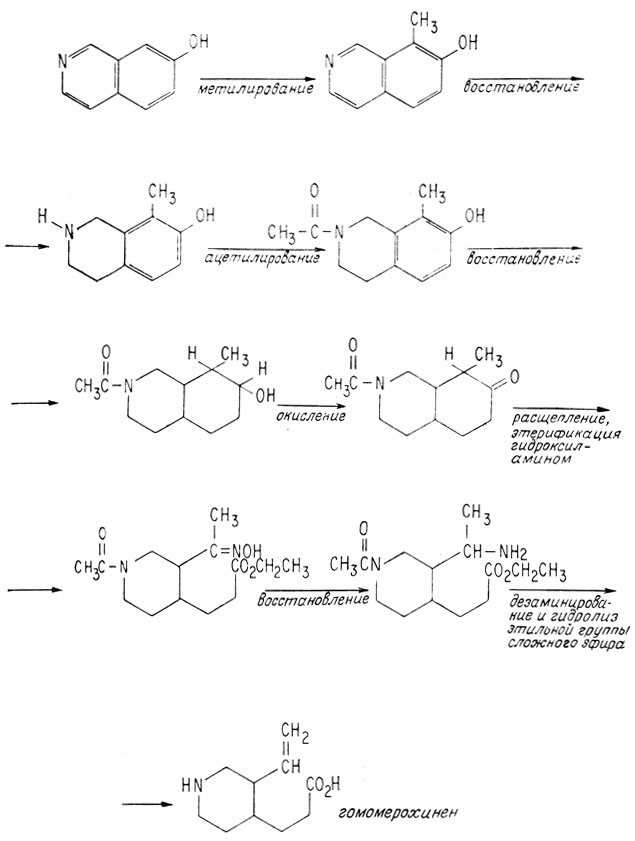
Превращением гомомерохинена в хинотоксин (аналогично тому, как это уже было проведено для дигидропроизводного) завершился полный синтез хинина. Таким образом, осуществились юношеские честолюбивые стремления Р. Вудворда, который удостоился за свою работу Нобелевской премии и стал признанным мастером в области органического синтеза.
Поскольку попытки получить новые более легко синтезируемые вещества, обладающие противомалярийным действием, не прекращались, вполне естественным было стремление выяснить, какие же участки молекулы хинина ответственны за его противомалярийную активность. Довольно сенсационным (учитывая интенсивные попытки получения хинина в начале 40-х годов) явилось открытие, что восстановление винильной группы, приводящее к дигидрохинину, не изменяет значительно противомалярийной активности хинина.
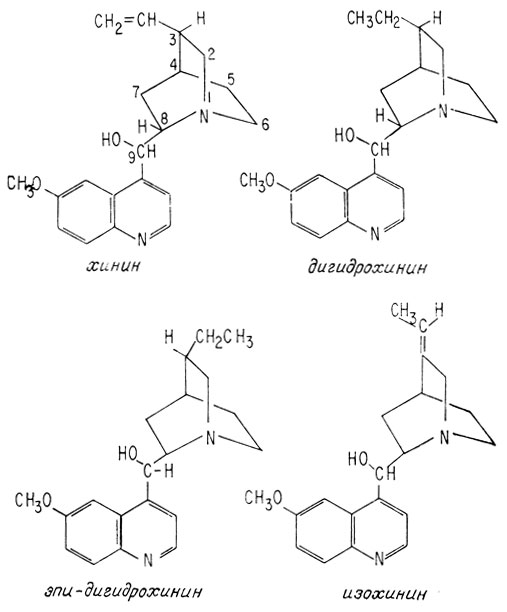
Даже при обращении конфигурации атома углерода в положении 3, в результате чего образуется эпи-дигидрохинин, молекула сохраняет свою противомалярийную активность. Более того, миграция двойной связи, при которой образуется изохинин, мало влияет на противомалярийные свойства. Однако при обращении конфигурации атома углерода в положении 9 (входящего в карбинольную группу), в результате чего образуется эпи-хинин, молекула утрачивает способность оказывать противомалярийное действие. Для противомалярийной активности важна также связь между атомом углерода в положении 8 и атомом азота, входящим в хинуклидиновую часть молекулы. Разрыв этой связи превращает хинин в неактивное производное пиперидина.
|
ПОИСК:
|
© BIOLOGYLIB.RU, 2001-2020
При копировании ссылка обязательна:
http://biologylib.ru/ 'Библиотека по биологии'
При копировании ссылка обязательна:
http://biologylib.ru/ 'Библиотека по биологии'