
Каким образом антибиотики уничтожают микробы
Век антибиотиков поставил перед микробиологами целый ряд вопросов. Рассмотрим один из них. Каким образом антибиотик убивает чувствительные к нему микробы? Уже Эрлих показал, что существует тесная связь между химической структурой "волшебной пули" и ее действием. В химическом отношении антибиотики - вещества очень разнообразные, хотя некоторые из них и являются производными какого-нибудь одного химического соединения, например тетрациклина. Можно ли утверждать, что вещества, сходные по своей химической структуре, сходны и по характеру своего действия на клетки и, напротив, различиям в строении сопутствуют и различия в антибиотических свойствах? Данные, полученные к настоящему времени, позволяют нам дать ответ на этот вопрос.
Теперь уже доподлинно известно, что пенициллин действует на клеточную стенку бактерий и препятствует ее синтезу. Некоторое время бактерии еще размножаются, но, лишенные клеточной стенки, очень скоро погибают.
Стрептомицин, проникнув в клетку, достигает рибосом - места синтеза белков - и блокирует их деятельность. Несколько по-иному действуют на синтез белков тетрациклины, эритромицин, хлорамфеникол и многие другие антибиотики, но каждый своим, только ему свойственным способом, который определяется особенностями строения его молекул.
Актиномицин, первый антибиотик Ваксмана, действует на молекулу ДНК. В результате становится невозможным синтез информационной РНК, переносящей к рибосомам "приказы" ДНК о синтезе белков. Сходное действие проявляет и рифампицин, хотя и несколько иным способом - снижает активность ферментов полимеразы РНК, и РНК не может образоваться.
На ДНК действуют и молекулы противоопухолевого антибиотика митомицина C: прочно связываясь с ней, они препятствуют дальнейшему синтезу ДНК.
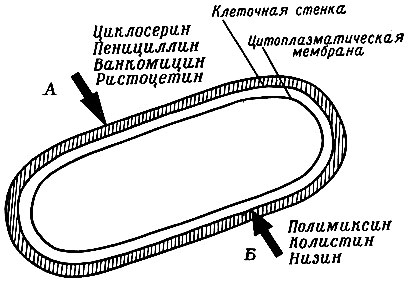
Пенициллин и ряд других антибиотиков препятствуют образованию клеточных стенок у растущих бактерий (А). Лишенные стенок бактерии постепенно превращаются в протопласты. Другие антибиотики нарушают функции цитоплазматической мембраны бактерии (Б)
Но все это лишь некоторые из наиболее известных и типичных механизмов действия антибиотиков на клетки микробов.
При повторных воздействиях молекул антибиотика клетка микроба погибает. Если же антибиотик вводится в малых количествах или поражает такую часть клетки, которая может быть легко восстановлена, микробы выживают.
Исследователь Л. Эбрингер (естественный факультет в Братиславе) наблюдал интересные явления, изучая действие стрептомицина, эритромицина и многих других антибиотиков на клетки Euglena gracilis. Этот организм способен к фотосинтезу и поэтому на свету не нуждается в органическом питании. Если же на E. gracilis подействовать упомянутыми антибиотиками, то фотосинтез прекращается. Процесс фотосинтеза происходит, как известно, в хлоропластах. Антибиотики полностью уничтожают хлоропласта эвглены, и дальнейшие ее генерации существуют уже без хлоропластов. Не будучи в состоянии осуществлять фотссинтез, они потребляют, естественно, лишь готовые органические соединения.
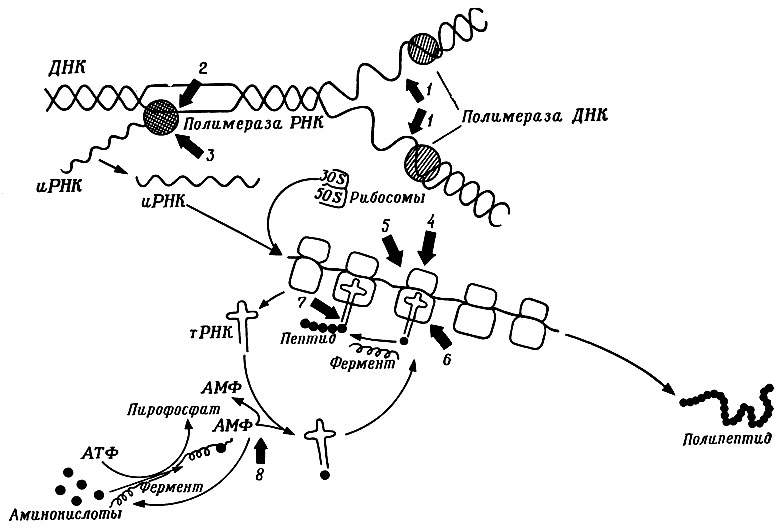
Действие антибиотиков на синтез нуклеиновых кислот и белков. Митомицин C (1), связываясь с молекулой ДНК, делает невозможным процесс ее редупликации под действием полимеразы ДНК и других ферментов. Актиномицин D (2), связываясь с молекулой ДНК, препятствует синтезу иРНК с помощью полимеразы РНК. Рифампицин (3) соединяется с полимеразой РНК и тоже предотвращает синтез иРНК. Вдоль молекулы иРНК группируются рибосомы, образуя полисомы, на которых возникают пептиды. Тетрациклин (4), связываясь с 30 S-субъединицами рибосом, лишает их возможности синтеза пептидов. Таким же образом связывается с ними и стрептомицин, вызывая 'неправильное прочтение' генетических записей на иРНК, в результате чего возникают пептиды с аномальным распределением аминокислот. Фузидиновая кислота (5) препятствует перемещению рибосом по молекуле иРНК, делая невозможным добавление дальнейших аминокислот к 'растущему' пептиду. Эритромицин и хлорамфеникол (5) связываются с 50 S-субъединицами рибосом и препятствуют деятельности тРНК, несущих с собой аминокислоты, которые необходимы для пополнения пептидов. Пуромицин (7) слишком рано отделяет пептиды от полисом, затрудняя тем самым синтез белков. Борелидин (8) препятствует присоединению 'активированных' аминокислот к тРНК, что делает невозможным их перемещение к полисомам
Мы наблюдали интересное действие антибиотиков на грибы. Оказывается, цианеин, первый из полученных нами антибиотиков (фиг. VIII), влияет нарост гриба Paecilomyces viridis. Как мы уже рассказывали, Ж. Сегретен из Пастеровского института выделил этот гриб из организма больных хамелеонов и доказал, что именно он был причиной их болезни и гибели. В пробирке гриб образует волокнистый мицелий, а в теле хамелеона-дрожжеподобные комочки. При помощи цианеина нам удалось "принудить" гриб образовывать дрожжеподобные формы и в пробирке.
Мы испытывали также действие цианеина на гриб Botrytis cinerea, паразитирующий на виноградной лозе. Гифы этого гриба на агаровых пластинках растут довольно хорошо, а разветвляются очень редко. В присутствии цианеина их рост замедляется, но зато они начинают сильно ветвиться. На рост гиф этого гриба влияют также и некоторые другие антибиотики (фото 63).
Эти морфологические изменения имеют довольно глубокие причины. Антибиотики влияют на ход биохимических процессов в клетках грибов, что проявляется в изменении характера роста.
|
ПОИСК:
|
© BIOLOGYLIB.RU, 2001-2020
При копировании ссылка обязательна:
http://biologylib.ru/ 'Библиотека по биологии'
При копировании ссылка обязательна:
http://biologylib.ru/ 'Библиотека по биологии'