
Пенициллин и другие антибиотики
Другим колоссальным шагом вперед на пути использования органических молекул в медицине явилось открытие антибиотика пенициллина. Обычно антибиотиком называют вещество, синтезируемое микроорганизмом и способное препятствовать развитию другого микроорганизма (или же убивать его).
Счастливая случайность позволила английскому бактериологу Александру Флемингу в 1929 г. впервые наблюдать противомикробную активность пенициллина. Культуры стафилококка, выращивавшиеся на обычной питательной среде, называемой агаром, случайно были заражены зеленой плесенью. Флеминг заметил, что по мере развития зеленой плесени стафилококковые палочки, находящиеся по соседству с плесенью, разрушались. Затем он обнаружил, что сама питательная среда, в которой развивалась плесень, не причиняла вреда лейкоцитам крови, и предположил, что содержащееся в плесени активное начало может быть использовано в качестве антисептика. Впоследствии было установлено, что плесень эта относится к виду Penicillium notation, однако в то время возможность использования выделяемого ею вещества для лечения общих инфекционных заболеваний не была исследована.
За несколько лет до начала второй мировой войны Х. Флори и Е. Чейн в Оксфорде решили разобраться в причинах этого явления. В 1940 г. они выделили натриевую соль пенициллина, содержащую примеси. При работе с зараженными мышами им удалось показать, что полученное вещество обладает замечательной противостафилококковой активностью. В начале 1941 г. пенициллин был впервые опробован на человеке - им был заболевший оксфордский полицейский, - и начался путь этого антибиотика к славе.
Война привела к тому, что пенициллин стал продуктом, имеющим стратегическое значение, поэтому исследования в Англии и США проводились в обстановке строгой секретности. Первой целью этих исследований было ферментативное получение антибиотика в больших количествах. Однако попытка установить структуру этой молекулы на молекулярном уровне в надежде, что, возможно, ее легче будет получить в чистом виде синтетическим путем, не увенчалась успехом. Хотя молекула пенициллина сравнительно невелика и не особенно сложна, в годы войны это вещество заставило поломать головы химиков-органиков, занимающихся вопросами структуры. Лишь в 1945 г., и то только с помощью рентгеноструктурного анализа (гл. 11), удалось, наконец, нащупать правильную структуру. Основная трудность состояла в получении (и сохранении) чистых образцов вследствие того, что молекула чрезвычайно чувствительна даже к малейшему изменению экспериментальных условий. Такая подвижность молекулы, как оказалось, обусловлена в первую очередь наличием в ней четырехчленной циклической амидной группы, что весьма неожиданно и во что даже трудно поверить. Никогда раньше такая β-лактамная структура в природных соединениях не была обнаружена.
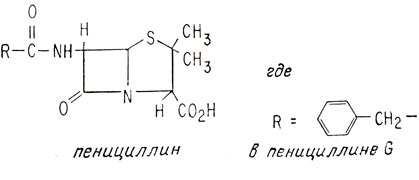
После установления структуры стало очевидно, что даже если бы она и стала известна раньше, синтетическое производство этого антибиотика наладить не удалось бы.
Различные виды плесени Penicillium выделяют молекулы пенициллина разных типов, которые отличаются только боковой цепью R. Широко применяемый пенициллин, называемый пенициллином G, содержит в качестве боковой цепи бензильную группу (C6H5-CH2-), и его часто называют бензилпенициллином. По существу, сердцем молекулы является бициклический фрагмент, известный под названием 6-аминопенициллановой кислоты
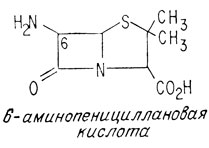
Эту молекулу можно считать производным двух встречающихся в природе аминокислот - цистеина и валина
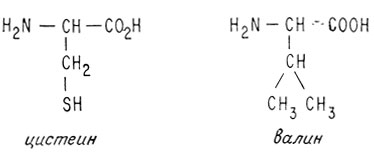
Сходство между этими двумя аминокислотами и 6-аминопенициллановой кислотой наиболее отчетливо видно, если расположить эти молекулы так, как показано ниже:
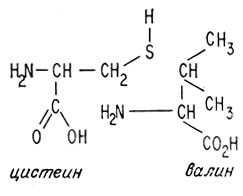
Химическое разложение пенициллина интенсивно изучалось в процессе исследования его структуры. Установлено, что при разложении пенициллина образуются не две эти кислоты, а соединения, близкие к ним по структуре. При гидролизе пенициллина в мягких условиях наиболее уязвимая часть молекулы - кольцо β-лактама - раскрывается с образованием дикарбоновой кислоты, называемой пенициллоиновой кислотой
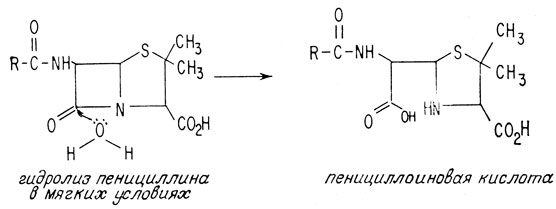
Некоторые бактерии, особенно из числа грамотрицательных, содержат фермент, называемый пенициллиназой, который и осуществляет подобный процесс. Поскольку пенициллиновая кислота не обладает антибиотической активностью, эти бактерии иммунны по отношению к действию пенициллина.
При взаимодействии пенициллоиновой кислоты с хлоридом одновалентной ртути отщепляется валинтиол (называемый пеницилламином).
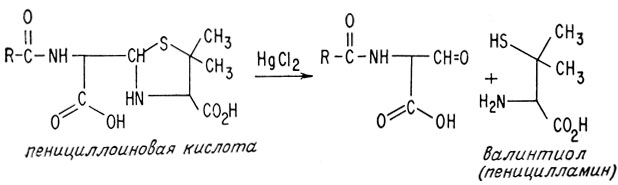
После того как были окончательно установлены структуры пеницилламина и другого фрагмента, были предложены три возможные структуры пенициллина, которые основывались на трех наиболее вероятных продуктах рекомбинации этих двух фрагментов. Лишь одна из этих структур включала β-лактамное кольцо. Однако имевшаяся в то время информация не давала возможности сделать окончательный выбор структуры для этого антибиотика. Вскоре методом рентгеноструктурного анализа было показано, что правильной является структура, содержащая кольцо β-лактама.
В последующие годы было сделано много попыток выяснить, как же действует пенициллин на бактерии. Как и для сульфаниламида, в настоящее время многое стало известно, и так же, как для сульфаниламида, механизм действия основан на различии между бактериальной и животной клетками.
Клеточная стенка бактерии должна быть такой, чтобы наряду с выполнением других функций она защищала бактерию от изменений осмотического давления в окружающей среде. Животные клетки не имеют стенок, они имеют лишь клеточные мембраны. Пенициллин препятствует образованию новых клеточных стенок, необходимых для роста и размножения бактерий. Нарушение стенки клетки (или ее отсутствие) может привести к разрыву бактериальной клетки и выливанию ее содержимого в окружающее пространство. Это может также позволить естественным защитным веществам организма, антителам, проникнуть в бактерию и уничтожить ее.
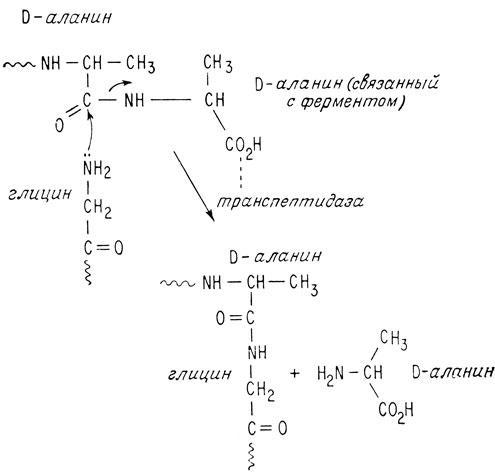
Пенициллин эффективен особенно и почти исключительно против грамположительных организмов. На одной из стадий образования клеточных стенок грамположительной бактерии фермент, называемый транспептидазой, вызывает образование пептидной связи между карбоксильной группой D-аланина* и аминогруппой глицина. Это реакция образования поперечной связи между двумя короткими пептидными цепями. В ходе этой реакции от конца цепи отделяется молекула D-аланина. Возможно, что эта концевая молекула D-аланина (имеющая свободную карбоксильную группу) присоединяется к активному центру фермента транспептидазы.
* (Как было показано выше, обычно кирпичиками, из которых строятся белки, являются L-аминокислоты. Однако в некоторых бактериях встречаются D-аминокислоты.)
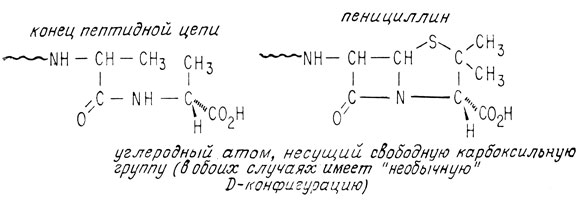
При рассмотрении механизма действия пенициллина важно отметить то обстоятельство, что имеющий свободную карбоксильную группу аланин, присоединяющийся к ферменту транспептидазе, обладает "необычной" D-конфигурацией. Она соответствует конфигурации углеродного атома, несущего карбоксильную группу в пенициллине. Такое сходство геометрии, а также другие доказательства приводят к представлению, что пенициллин включается в процесс образования клеточной стенки, связываясь с транспептидазой и инактивируя этот фермент, необходимый для образования поперечной связи между пептидными цепями.
Клеточные стенки грамотрицательных бактерий не окрашиваются при действии на них красителя Грама. Это свидетельствует о том, что структуры стенок клеток грамотрицательных и грамположительных бактерий неодинаковы. Различная структура клеточных стенок, вероятно, требует разных ферментов для их построения. Таким образом, обычно наблюдаемую неэффективность пенициллина по отношению к грамотрицательным бактериям можно было бы объяснить неучастием грамположительного фермента транспептидазы при построении стенок клеток грамотрицательных бактерий.
|
ПОИСК:
|
© BIOLOGYLIB.RU, 2001-2020
При копировании ссылка обязательна:
http://biologylib.ru/ 'Библиотека по биологии'
При копировании ссылка обязательна:
http://biologylib.ru/ 'Библиотека по биологии'