
Реакция Фельгена с реактивом Шиффа на ДНК
Реакция Фельгена указывает на присутствие ДНК, поэтому она прежде всего может быть использована для констатации наличия или отсутствия ядер в клетках, их размеров, формы, местоположения и т. д. Кроме того, интенсивность окрашивания может дать косвенные указания на количественные изменения ДНК.
Реактив Шиффа - фуксинсернистая кислота - является характерным реактивом на альдегиды. На свойстве реактива Шиффа взаимодействовать с альдегидными группами основана и реакция Фельгена с этим реактивом на ДНК. Однако, ввиду того что в молекуле ДНК альдегидные группы связаны, их надо предварительно освободить. Это достигается проведением гидролиза ДНК слабой кислотой, в результате которого происходит отщеплейие пуриновых оснований (аденина, гуанина) от молекулы ДНК и образуется остаток молекулы ДНК со свободными альдегидными группами:
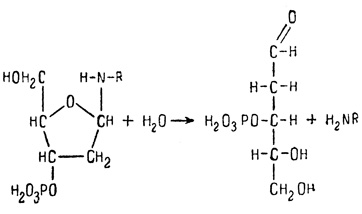
Изменения возникают у первого углеродного атома дезоксирибозы; в месте отрыва пуриновых оснований выявляется потенциальная альдегидная группа. При. этом фуранозная форма дезоксирибозы превращается в форму нециклического сахара. В процессе реакции к двум альдегидным группам дезоксирибозы присоединяется одна молекула фуксинсернистой кислоты.
Фуксинсернистая кислота (лейкофуксин) получается из кислого раствора основного фуксина (парафуксина) в 1 н. соляной кислоте при насыщении его сернистым ангидридом. Сернистый ангидрид образуется при взаимодействии соляной кислоты с бисульфитом натрия, которые вносятся в кислый раствор основного фуксина:
HCl+NaHSO3=NaCl+SO2+H2O
При пропускании сернистого газа в раствор фуксина нарушаются две двойные связи, в одном из трех ароматических колец фуксина исчезает хиноидная группировка, а вместе с ней и лилово-красная окраска, свойственная фуксину. Фуксинсернистая кислота - непрочное бесцветное соединение.
Получение фуксинсернистой кислоты из основного фуксина протекает следующим образом: фуксин, взаимодействуя с соляной кислотой, образует комплексное соединение, которое далее реагирует с сернистой кислотой по следующей схеме:
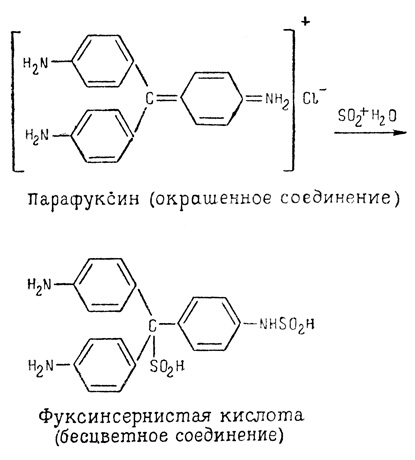
Таким образом, при образовании фуксинсернистой кислоты к фуксину присоединяются две группы (-SO2H).
При реакции с альдегидами хиноидная группировка восстанавливается, так как фуксинсернистая кислота - неустойчивое соединение, разлагается с образованием сернистой кислоты.
При взаимодействии одной молекулы фуксинсернистой кислоты с двумя молекулами остатков ДНК, имеющих обнаженные альдегидные группы, получается одна молекула окрашенного соединения.
При подготовке материала для проведения реакции Фельгена обычно рекомендуют фиксацию в спиртовых и кислых фиксаторах. Чаще всего применяют фиксатор Карнуа (стр. 45). Такой фиксатор осаждает нуклеопротеиды, что приводит к удачным морфологическим картинам. Однако длительное пребывание материала в фиксаторе вызывает разрушение связи между нуклеиновыми кислотами и белками, приводит к постепенной экстракции нуклеиновых кислот и дает искаженную картину. Поэтому пребывание в фиксаторе надо максимально ограничивать.
Реактивы
1) Реактив Шиффа (фуксинсернистая кислота).
Приготовление реактива Шиффа. 1 г основного фуксина растереть в ступке и растворить в 200 мл кипящей дистиллированной воды; охладить до 50°С. В охлажденный раствор добавить 20 мл 1 н. соляной кислоты* и охладить до 25°С. Добавить 1 г бисульфита или метабисульфита натрия. Полученную смесь взболтать с активированным углем (от 1 да 3 мин) и профильтровать. Налить в темный или завернутый в темную бумагу сосуд, закрыть его притертой пробкой и поместить в темноту на 12 или более часов до обесцвечивания основного фуксина и образования фуксинсернистой кислоты.
* (1 н. соляная кислота соответствует 10%-ному раствору, приготовленному из концентрированной соляной кислоты (уд. в. 1,19))
2) Сернистая вода.
Приготовление сернистой воды. К 200 мл дистиллированной воды добавить 20 мл 1 н. соляной кислоты и 1 г бисульфита натрия.
3) 1 н. соляная кислота.
4) Среды для обезвоживания объектов и заключения их в канадский бальзам (стр. 66-70).
5) Канадский бальзам.
Проведение реакции
* (См. сноску на стр. 118.)
1. Погрузить препараты в 1 н. соляную кислоту на несколько секунд.
2. Перенести их в заранее нагретую до 60° С 1 н. HCl и поместить в термостат при температуре 60° С (или на водяную баню с такой же температурой) на 5-10 мин*.
* (Длительность гидролиза зависит от примененного фиксатора. При употреблении фиксатора Карнуа и формалина оптимальное время 8 мин.)
3. Сполоснуть препараты холодной 1 н. HCl.
4. Поместить их в реактив Шиффа на 1 ч.
5. Отмыть избыток реактива Шиффа сернистой водой (3 смены по 3-5 мин).
6. Промывать препараты в водопроводной воде в течение 5-10 мин, сменяя начинающую розоветь воду.
7. Довести препараты до бальзама через 96%-ный, 100%-ный спирт, смесь спирта с ксилолом и ксилол.
8. Наблюдать появление малиновой окраски.
Результаты реакции (табл. 20)
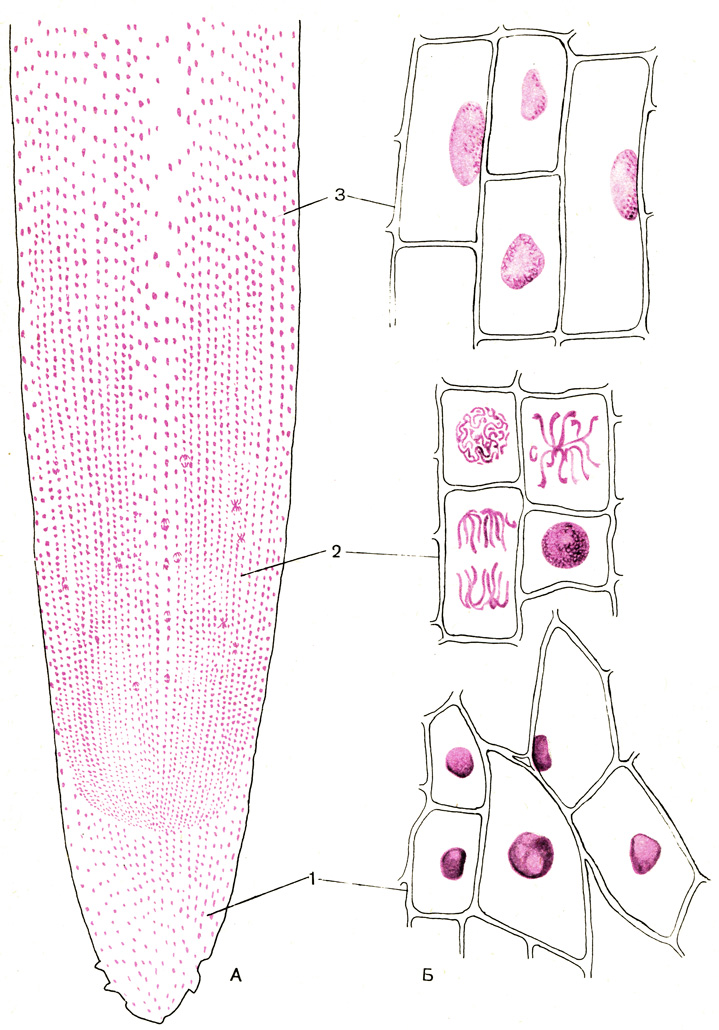
Таблица 20. Реакция Фельгена. Кончик корешка лука. А - общий вид кончика корешка лука в разрезе; Б - детали строения кончика порошка лука; 1 - корневой чехлик; 2 - зона деления; 3 - зона растяжения (увеличение 7 X 8 и 7 X 40)
В кончике корешка лука ядра приобретают малиново-фиолетовую окраску. Ядра зоны растяжения и особенно всасывания выглядят несколько менее яркими, чем ядра зоны деления. Ядрышки, цитоплазма и оболочки клеток остаются неокрашенными.
В зерновке кукурузы ядра корешка, почечки и всех остальных тканей зародыша, а также клеток алейронового слоя окрашиваются в характерный для реакции Фельгена цвет. Сплюснутые и растянутые ядра клеток эндосперма окрашиваются более бледно.
|
ПОИСК:
|
© BIOLOGYLIB.RU, 2001-2020
При копировании ссылка обязательна:
http://biologylib.ru/ 'Библиотека по биологии'
При копировании ссылка обязательна:
http://biologylib.ru/ 'Библиотека по биологии'